Il prodotto diretto della calcinazione è un materiale solido che è stato purificato termicamente o alterato chimicamente. Il processo utilizza un calore elevato in un ambiente a basso contenuto di ossigeno per eliminare sostanze volatili come acqua e anidride carbonica, decomporre composti o modificare la struttura cristallina del materiale senza fonderlo.
La calcinazione non è una fase finale di produzione, ma un processo preparatorio cruciale. Il suo scopo principale è trasformare un solido grezzo e impuro in un materiale più concentrato, stabile o reattivo, ottimizzato per un processo successivo come la fusione o la sintesi chimica.

Cosa cambia durante la calcinazione?
La calcinazione raggiunge il suo obiettivo inducendo cambiamenti fisici e chimici specifici in un materiale attraverso un riscaldamento attentamente controllato. Il prodotto è definito da quale di queste trasformazioni avviene.
Decomposizione Termica
Questo è l'obiettivo più comune della calcinazione. Il calore scompone un composto chimico in due o più sostanze più semplici.
Un esempio classico è la produzione di calce dalla pietra calcarea. Il riscaldamento del carbonato di calcio (CaCO3) elimina l'anidride carbonica (CO2), lasciando dietro di sé l'ossido di calcio (CaO), o calce viva.
Rimozione delle Frazioni Volatili
La calcinazione è molto efficace nel rimuovere le impurità volatili intrappolate all'interno del solido. Ciò purifica e concentra il materiale desiderato.
Ciò include la rimozione dell'acqua fisicamente assorbita (essiccazione) e, cosa più importante, delle molecole d'acqua legate chimicamente dai minerali idrati, un processo noto come disidratazione.
Induzione di una Transizione di Fase
A volte, l'obiettivo non è cambiare la composizione chimica, ma alterare la struttura cristallina interna del materiale, ovvero la fase.
Il riscaldamento di un materiale può causare la riorganizzazione dei suoi atomi in una forma cristallina diversa, spesso più stabile o utile. Questo è un passaggio comune nella produzione di specifici tipi di ceramiche e catalizzatori.
L'Obiettivo: Preparare i Materiali per il Passo Successivo
Comprendere il prodotto della calcinazione richiede di vederla come un mezzo per un fine. Il solido risultante è raramente il prodotto finale, ma è ora pronto per un'applicazione industriale più impegnativa.
Aumento della Concentrazione del Minerale
In metallurgia, la calcinazione viene utilizzata per trattare i minerali prima della fusione. Eliminando l'acqua dagli ossidi idrati o l'anidride carbonica dai minerali carbonatici, il processo rimuove il peso morto.
Ciò aumenta significativamente la percentuale di metallo nel minerale, rendendo il successivo processo di fusione, ad alta intensità energetica, più efficiente ed economico.
Creazione di un Materiale Più Reattivo
Il prodotto calcinato è spesso più reattivo chimicamente rispetto al materiale grezzo originale.
La calce (ossido di calcio) prodotta dalla calcinazione della pietra calcarea è un ingrediente chiave nella produzione di cemento proprio perché reagisce prontamente con altri componenti. La pietra calcarea originale non lo fa.
Comprendere le Distinzioni Chiave
Per comprendere veramente ciò che produce la calcinazione, è fondamentale distinguerla da processi simili ad alta temperatura che hanno obiettivi e risultati diversi.
Calcinazione vs. Arrostimento
La differenza fondamentale è la presenza di aria. La calcinazione avviene in assenza o in quantità limitata di aria per causare la decomposizione termica.
L'arrostimento, al contrario, è il riscaldamento in eccesso di aria. Il suo scopo è indurre l'ossidazione, convertendo tipicamente i minerali solfuri metallici in ossidi metallici.
Calcinazione vs. Sinterizzazione
Questi processi hanno obiettivi fisici opposti. La calcinazione mira a purificare o decomporre un materiale, rendendolo spesso più poroso o polveroso.
La sinterizzazione utilizza il calore per fondere piccole particelle insieme in un unico pezzo solido, aumentandone la resistenza e la densità senza fonderlo.
Applicare la Calcinazione in Modo Efficace
Il prodotto desiderato determina come e quando utilizzare questo processo. La tua scelta dipende interamente dal materiale di partenza e dal tuo obiettivo finale.
- Se il tuo obiettivo principale è produrre calce o cemento: Utilizza la calcinazione per la decomposizione termica della pietra calcarea (carbonato di calcio) in calce (ossido di calcio).
- Se il tuo obiettivo principale è preparare un minerale metallico per la fusione: Applica la calcinazione per rimuovere acqua o anidride carbonica, concentrando così l'ossido metallico desiderato.
- Se il tuo obiettivo principale è sviluppare proprietà specifiche del materiale: Utilizza la calcinazione per controllare con precisione la transizione di fase e la struttura cristallina del tuo materiale grezzo, una pratica comune nella produzione di ceramiche e catalizzatori.
In definitiva, la calcinazione è il processo di trattamento termico fondamentale per purificare e preparare i materiali solidi per la loro applicazione finale.
Tabella Riassuntiva:
| Obiettivo del Processo | Materiale di Partenza | Materiale Prodotto | Cambiamento Chiave |
|---|---|---|---|
| Decomposizione Termica | Pietra Calcarea (CaCO₃) | Calce Viva (CaO) | Elimina CO₂ |
| Rimozione dei Volatili | Minerale Idrato | Minerale Concentrato | Rimuove acqua/impurità |
| Transizione di Fase | Precursore Ceramico | Ceramica Stabile | Modifica la struttura cristallina |
Hai bisogno di un'elaborazione termica precisa per i tuoi materiali? Le attrezzature avanzate per la calcinazione di KINTEK sono progettate per laboratori e applicazioni industriali, garantendo purezza, reattività e controllo di fase ottimali per minerali, ceramiche e precursori chimici. Contatta oggi i nostri esperti per discutere come le nostre soluzioni possono migliorare il tuo processo di preparazione dei materiali.
Guida Visiva
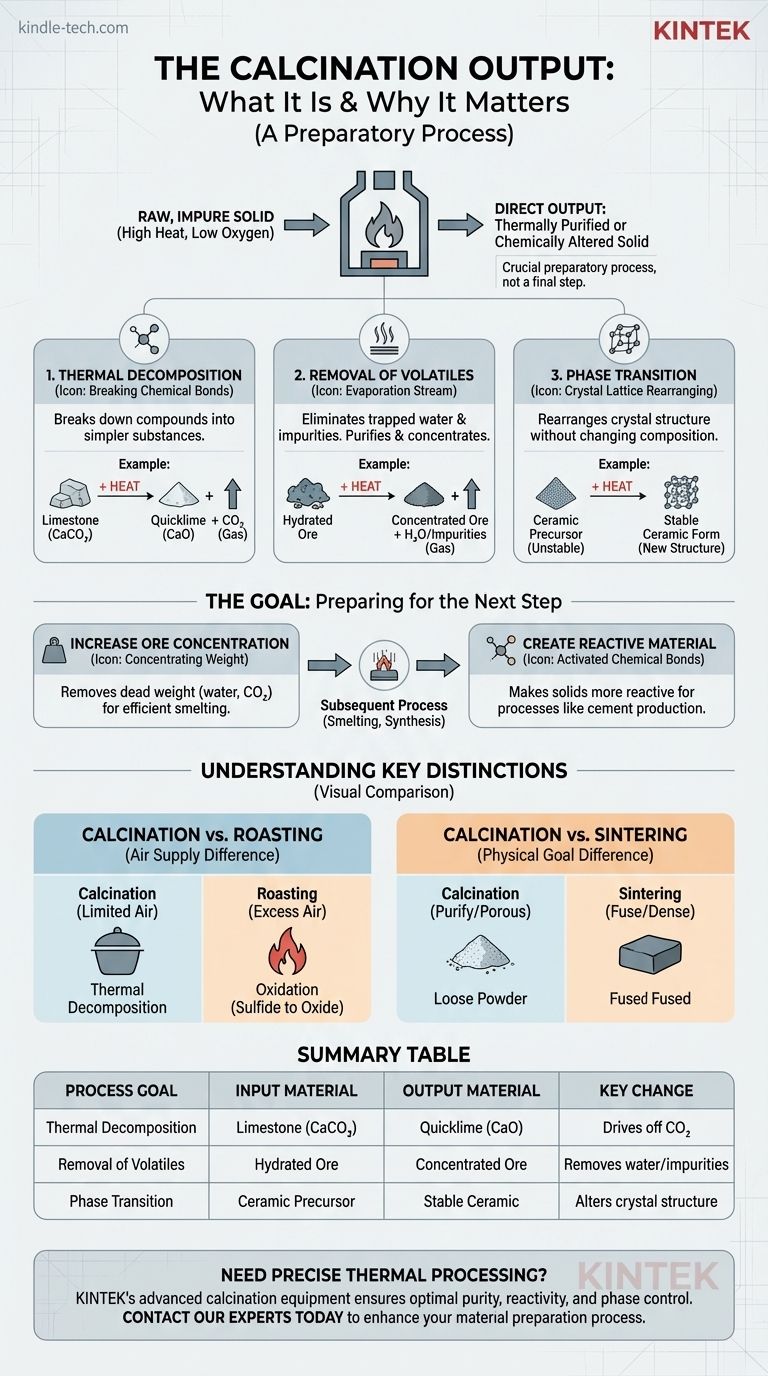
Prodotti correlati
- Impianto di pirolisi a forno rotante elettrico Macchina Calcinatore Piccolo Forno Rotante Forno Rotante
- Fornace a Pirolisi Continua Elettrica Rotante per Lavorazione Piccola Scala
- Fornace a fusione a induzione ad arco sotto vuoto non consumabile
- Fornace di grafitazione sottovuoto verticale ad alta temperatura
- Fornace di grafitazione sottovuoto a temperatura ultra-elevata in grafite
Domande frequenti
- Come vengono riscaldati i forni rotativi? Spiegazione dei metodi di riscaldamento diretto e indiretto
- Il forno rotante è un forno? Scopri le differenze chiave per la lavorazione industriale
- Qual è l'efficienza energetica di un forno rotante? Raggiungere un'efficienza termica superiore al 95%
- Quali sono i diversi tipi di calcinatori? Una guida alla scelta dell'attrezzatura giusta per la lavorazione termica
- Quali sono le caratteristiche delle modalità di movimento del letto a scorrimento, cedimento e rotolamento? Ottimizza il tuo processo rotativo



















