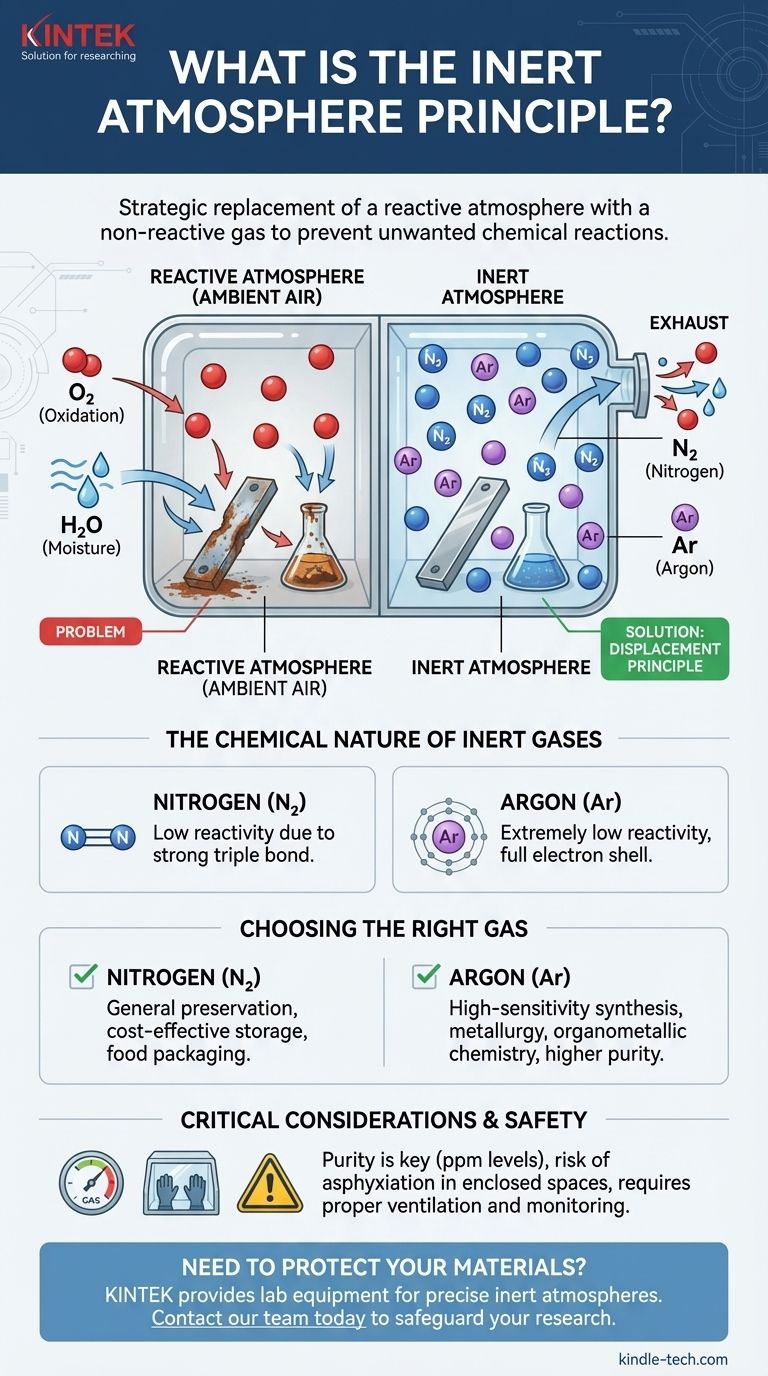
Il principio dell'atmosfera inerte è la sostituzione strategica di un'atmosfera reattiva, come l'aria ambiente, con un gas non reattivo (inerte). Ciò viene fatto per creare un ambiente controllato che prevenga reazioni chimiche indesiderate, come l'ossidazione e il degrado indotto dall'umidità. I gas inerti più comuni utilizzati a questo scopo sono l'azoto e l'argon, che spostano ossigeno e vapore acqueo da un sistema.
L'obiettivo di un'atmosfera inerte non è aggiungere un ingrediente speciale, ma rimuovere quelli problematici. Spostando sistematicamente gas reattivi come ossigeno e acqua, si crea un ambiente stabile che protegge i materiali sensibili e assicura che i processi chimici procedano senza interferenze.

Il Problema: Reattività Atmosferica Incontrollata
L'aria normale, l'ambiente in cui esistiamo, è una miscela chimica sorprendentemente reattiva. Per molti processi scientifici e industriali, questa reattività è un problema significativo.
Perché l'aria normale è una sfida
La nostra atmosfera è composta da circa il 21% di ossigeno e quantità variabili di vapore acqueo. Entrambi questi componenti sono altamente reattivi e desiderosi di partecipare a reazioni chimiche.
L'ossigeno è un potente agente ossidante, il che significa che accetta prontamente elettroni da altre sostanze. Questa è la causa principale di processi comuni come la ruggine e la combustione.
L'Impatto dell'Ossidazione e del Degrado
Quando i materiali sensibili sono esposti all'aria, possono degradarsi rapidamente. Ad esempio, l'ossigeno può rovinare un delicato esperimento elettrochimico reagendo sulla superficie dell'elettrodo, oscurando i risultati che si stanno cercando di misurare.
Allo stesso modo, molti prodotti chimici avanzati, prodotti farmaceutici e reagenti si decompongono o perdono la loro potenza se esposti a ossigeno o umidità. Questo principio è anche il motivo per cui i produttori di alimenti confezionano prodotti come le patatine in sacchetti riempiti di azoto per impedire agli oli di irrancidire.
Come un'Atmosfera Inerte Risolve il Problema
Un'atmosfera inerte contrasta direttamente la minaccia della reattività atmosferica cambiando fisicamente l'ambiente a livello gassoso.
Il Principio di Spostamento
La tecnica fondamentale prevede la purga di un contenitore, di un recipiente di reazione o di una camera con un gas inerte. Mentre il gas inerte fluisce, spinge fisicamente fuori, o sposta, l'aria ambiente contenente ossigeno e vapore acqueo.
Ciò si ottiene spesso facendo gorgogliare il gas inerte (come argon o azoto) attraverso una soluzione liquida o lavando continuamente un contenitore sigillato, come una glovebox.
La Natura Chimica dei Gas Inerti
Gas come l'azoto (N₂) e l'argon (Ar) sono scelti perché sono estremamente non reattivi.
L'Argon è un gas nobile, il che significa che il suo guscio elettronico più esterno è completo. Non ha incentivi chimici a reagire con altri elementi.
Il gas azoto è una molecola biatomica (N₂) tenuta insieme da un triplo legame eccezionalmente forte. È necessaria una quantità significativa di energia per rompere questo legame, rendendo il gas azoto molto stabile e improbabile che partecipi alla maggior parte delle reazioni in condizioni normali.
Comprendere i Compromessi
Sebbene il principio sia semplice, la sua applicazione pratica comporta scelte importanti e potenziali sfide.
Scegliere il Gas Giusto: Azoto vs. Argon
L'Azoto è il cavallo di battaglia delle atmosfere inerti. È molto meno costoso dell'argon ed è sufficientemente inerte per la stragrande maggioranza delle applicazioni, dall'imballaggio alimentare allo stoccaggio chimico generale.
L'Argon è utilizzato per applicazioni altamente sensibili in cui non può essere tollerata nemmeno la minima reattività. È chimicamente più inerte dell'azoto e, essendo più denso dell'aria, può formare una "coperta" protettiva più stabile sopra un processo. Ciò lo rende ideale per la metallurgia ad alta temperatura e la sintesi organometallica sensibile.
La Sfida della Purezza
Basta una semplice purga del sistema una volta potrebbe non essere sufficiente. Anche tracce di ossigeno o vapore acqueo (misurate in parti per milione) possono essere sufficienti per interrompere esperimenti altamente sensibili o degradare materiali ultrapuri.
Ottenere e mantenere un alto livello di purezza spesso richiede una purga continua, una sigillatura meticolosa del sistema e talvolta l'uso di scrubber di ossigeno per rimuovere le ultime tracce residue.
Considerazioni Critiche sulla Sicurezza
I gas inerti sono semplici asfissianti. Non sono tossici, ma spostano l'ossigeno necessario per la respirazione. Lavorare in uno spazio chiuso in cui viene utilizzato un gas inerte può essere estremamente pericoloso e richiede una ventilazione adeguata e un monitoraggio continuo dell'ossigeno per prevenire l'asfissia.
Fare la Scelta Giusta per il Tuo Obiettivo
La selezione dell'approccio giusto dipende interamente dal tuo obiettivo, budget e requisiti di sensibilità.
- Se la tua attenzione principale è la conservazione generale o lo stoccaggio di massa: L'azoto è quasi sempre la scelta più conveniente e pratica per prevenire l'ossidazione.
- Se la tua attenzione principale è la sintesi ad alta sensibilità o l'elettrochimica: L'argon è la scelta superiore per la sua quasi totale mancanza di reattività, giustificando il suo costo più elevato.
- Se la tua attenzione principale è la lavorazione dei metalli ad alta temperatura: L'argon è essenziale, poiché l'azoto può reagire con alcuni metalli ad alte temperature per formare nitruri indesiderati.
In definitiva, padroneggiare il principio dell'atmosfera inerte significa controllare l'ambiente chimico per ottenere risultati prevedibili e affidabili.
Tabella Riassuntiva:
| Aspetto | Azoto (N₂) | Argon (Ar) |
|---|---|---|
| Uso Principale | Conservazione generale, stoccaggio conveniente | Sintesi ad alta sensibilità, processi ad alta temperatura |
| Reattività | Bassa (forte triplo legame) | Estremamente bassa (gas nobile) |
| Costo | Inferiore | Superiore |
| Ideale Per | Imballaggio alimentare, stoccaggio di prodotti chimici sfusi | Metallurgia, chimica organometallica, elettrochimica sensibile |
Hai bisogno di proteggere i tuoi materiali o processi dall'ossidazione?
In KINTEK, siamo specializzati nel fornire le attrezzature da laboratorio e i materiali di consumo giusti per creare e mantenere atmosfere inerti precise per la tua applicazione specifica. Sia che tu richieda una soluzione economica a base di azoto o un ambiente di argon ultrapuro per lavori sensibili, i nostri esperti possono aiutarti a selezionare il sistema ottimale.
Contatta il nostro team oggi stesso per discutere come possiamo salvaguardare la tua ricerca e produzione con soluzioni affidabili di atmosfera inerte.
Guida Visiva
Prodotti correlati
- Forno ad atmosfera controllata 1200℃ Forno ad atmosfera inerte ad azoto
- Fornace a atmosfera controllata da 1700℃ Fornace a atmosfera inerte di azoto
- Fornace a atmosfera controllata da 1400℃ con azoto e atmosfera inerte
- Fornace a Idrogeno Inertee Controllato all'Azoto
- Fornace a atmosfera controllata con nastro a maglie
Domande frequenti
- Qual è la funzione di un forno ad atmosfera controllata di alta precisione per la lega 617? Simulare condizioni estreme VHTR
- Qual è la funzione di un forno a atmosfera controllata? Nitrurazione Master per Acciaio AISI 52100 e 1010
- Cos'è un forno ad atmosfera controllata per il trattamento termico? Domina la Chimica e la Metallurgia delle Superfici
- È possibile brasare rame su ottone senza flussante? Sì, ma solo in queste condizioni specifiche.
- Come viene utilizzato l'ossigeno (O2) nelle atmosfere controllate del forno? Padronanza dell'ingegneria delle superfici per i metalli




