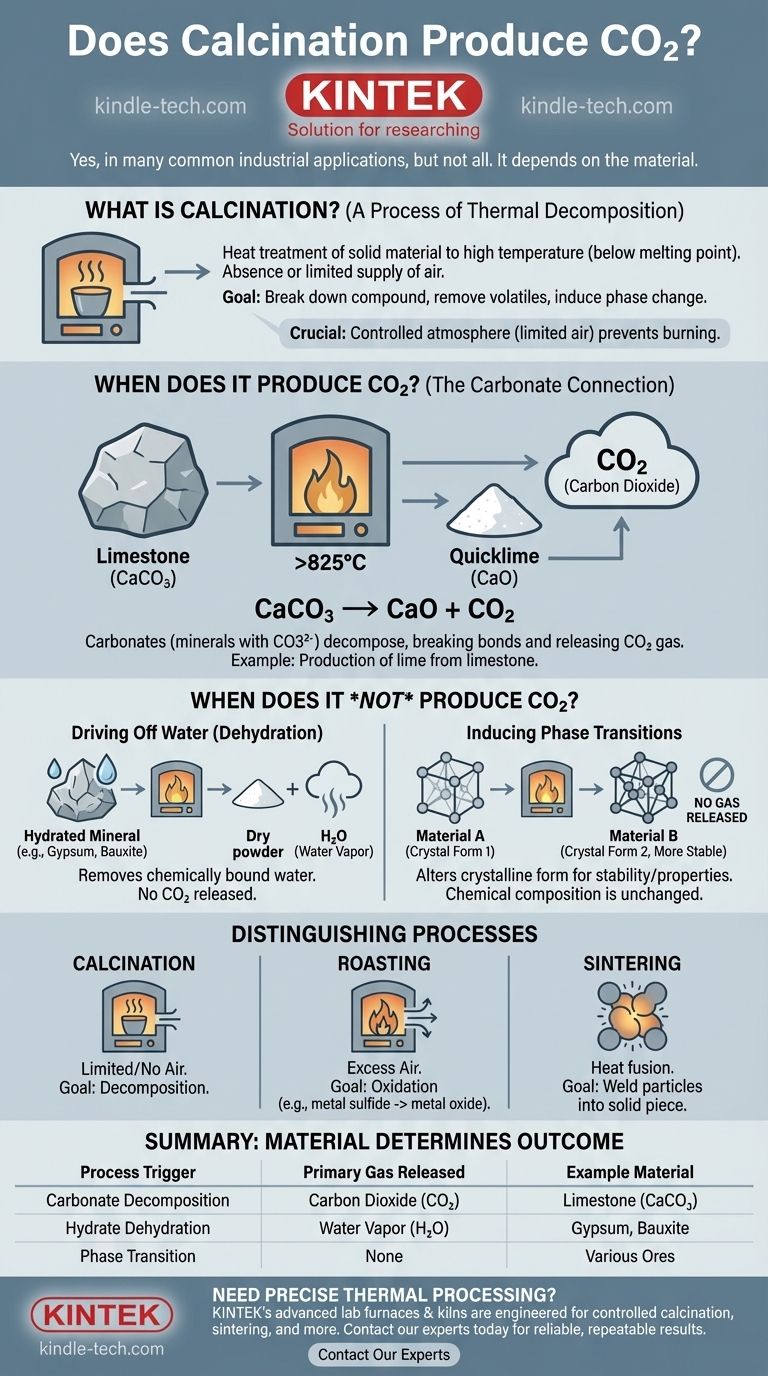
In molte comuni applicazioni industriali, sì. La calcinazione è un processo di riscaldamento e, quando applicata a materiali contenenti carbonati come il calcare, provoca una scomposizione chimica che rilascia quantità significative di anidride carbonica (CO2). La produzione di calce dal calcare è un esempio primario di questa reazione.
Il punto cruciale da capire è che la calcinazione è un processo, non una singola reazione specifica. Se produca CO2 dipende interamente dalla composizione chimica del materiale riscaldato.

Cos'è fondamentalmente la calcinazione?
Un processo di decomposizione termica
La calcinazione è un processo di trattamento termico in cui un materiale solido viene riscaldato a una temperatura elevata, ma al di sotto del suo punto di fusione. Ciò avviene in assenza o con una fornitura molto limitata di aria.
Lo scopo principale è indurre la decomposizione termica, il che significa scomporre il composto utilizzando il calore.
L'obiettivo: indurre un cambiamento
L'obiettivo della calcinazione non è sempre lo stesso. Può essere utilizzata per:
- Rimuovere una sostanza volatile, come la CO2 dal calcare o l'acqua da un minerale idrato.
- Rimuovere le impurità da un minerale.
- Causare una transizione di fase, modificando la struttura cristallina e le proprietà del materiale.
Il ruolo dell'atmosfera
L'atmosfera controllata (aria limitata) è cruciale. Impedisce al materiale di bruciare o ossidarsi, distinguendo la calcinazione da altri trattamenti termici come la tostatura.
Quando la calcinazione produce CO2?
Il legame con i carbonati
La calcinazione produce anidride carbonica quando la materia prima è un carbonato. I carbonati sono minerali che contengono lo ione carbonato (CO3²⁻).
Quando riscaldati, questi minerali si decompongono, rompendo i loro legami chimici e rilasciando gli atomi di carbonio e ossigeno come gas CO2.
Esempio: produzione di calce dal calcare
L'esempio più classico è la calcinazione del calcare (carbonato di calcio, CaCO₃).
Quando riscaldato a oltre 825°C (1517°F), si decompone in ossido di calcio (CaO), noto anche come calce viva, e rilascia anidride carbonica. La reazione chimica è: CaCO₃ → CaO + CO₂.
Altri minerali carbonatici
Questo principio si applica anche ad altri minerali carbonatici, come la magnesite (MgCO₃) o la dolomite (CaMg(CO₃)₂), che rilasciano anch'essi CO2 al riscaldamento.
Quando la calcinazione non produce CO2?
Eliminazione dell'acqua (disidratazione)
Molti minerali vengono calcinati semplicemente per eliminare l'acqua (H₂O) che è legata chimicamente all'interno della loro struttura cristallina.
Ad esempio, la calcinazione del minerale di bauxite per produrre allumina (ossido di alluminio) o il riscaldamento del gesso per produrre solfato di calcio emidrato (gesso) rilasciano entrambi vapore acqueo, non anidride carbonica.
Induzione di transizioni di fase
A volte, un materiale viene calcinato semplicemente per alterare la sua forma cristallina. Questo può renderlo più stabile, più reattivo o conferirgli proprietà fisiche diverse.
In questi casi, la composizione chimica non cambia e non viene rilasciato alcun gas.
Distinguere la calcinazione da processi simili
Calcinazione vs. Tostatura
La tostatura è il riscaldamento di un minerale in presenza di eccesso di aria. Il suo scopo è tipicamente l'ossidazione, come la conversione di un solfuro metallico in un ossido metallico. La calcinazione avviene in aria limitata o assente per causare decomposizione.
Calcinazione vs. Sinterizzazione
La sinterizzazione utilizza il calore per fondere piccole particelle in un unico pezzo solido, spesso dopo che le impurità sono già state rimosse. La calcinazione scompone un materiale; la sinterizzazione lo salda insieme.
Fare la scelta giusta per il tuo obiettivo
Comprendere il materiale di partenza è la chiave per prevedere il risultato.
- Se il tuo materiale è un carbonato (come calcare o dolomite): Aspettati una significativa produzione di CO2 come risultato principale del processo.
- Se il tuo materiale è un idrato (come bauxite o gesso): L'emissione principale sarà vapore acqueo (vapore), non CO2.
- Se il tuo obiettivo è modificare la struttura cristallina di un materiale: Il processo potrebbe non rilasciare alcun gas.
In definitiva, la calcinazione è uno strumento versatile definito dal calore e da un'atmosfera controllata, mentre i suoi risultati specifici sono dettati dalla chimica.
Tabella riassuntiva:
| Innesco del processo | Gas principale rilasciato | Materiale di esempio |
|---|---|---|
| Decomposizione del carbonato | Anidride carbonica (CO₂) | Calcare (CaCO₃) |
| Disidratazione dell'idrato | Vapore acqueo (H₂O) | Gesso, Bauxite |
| Transizione di fase | Nessuno | Vari minerali |
Hai bisogno di un'elaborazione termica precisa per i tuoi materiali? I forni e i forni da laboratorio avanzati di KINTEK sono progettati per la calcinazione controllata, la sinterizzazione e altro ancora. Sia che tu stia lavorando carbonati, idrati o altri materiali, le nostre apparecchiature garantiscono un controllo accurato della temperatura e una gestione dell'atmosfera per risultati affidabili e ripetibili. Contatta oggi i nostri esperti per trovare la soluzione termica perfetta per le esigenze specifiche del tuo laboratorio.
Guida Visiva
Prodotti correlati
- Impianto di pirolisi a forno rotante elettrico Macchina Calcinatore Piccolo Forno Rotante Forno Rotante
- Fornace a Pirolisi Continua Elettrica Rotante per Lavorazione Piccola Scala
- Fornace di grafitazione sottovuoto verticale ad alta temperatura
- Fornace di Grafittizzazione per Film ad Alta Conducibilità Termica al Vuoto di Grafite
- Fornace di grafitazione sottovuoto a temperatura ultra-elevata in grafite
Domande frequenti
- Qual è l'efficienza energetica di un forno rotante? Raggiungere un'efficienza termica superiore al 95%
- Qual è la temperatura di un forno rotante? Dipende dal tuo materiale e dall'obiettivo del processo
- Quali sono i principi di un forno rotante? Padroneggiare la meccanica della lavorazione ad alta temperatura
- Quali sono i diversi tipi di calcinatori? Una guida alla scelta dell'attrezzatura giusta per la lavorazione termica
- Quali sono i vantaggi del forno a tamburo rotante? Ottieni uniformità ed efficienza superiori



















