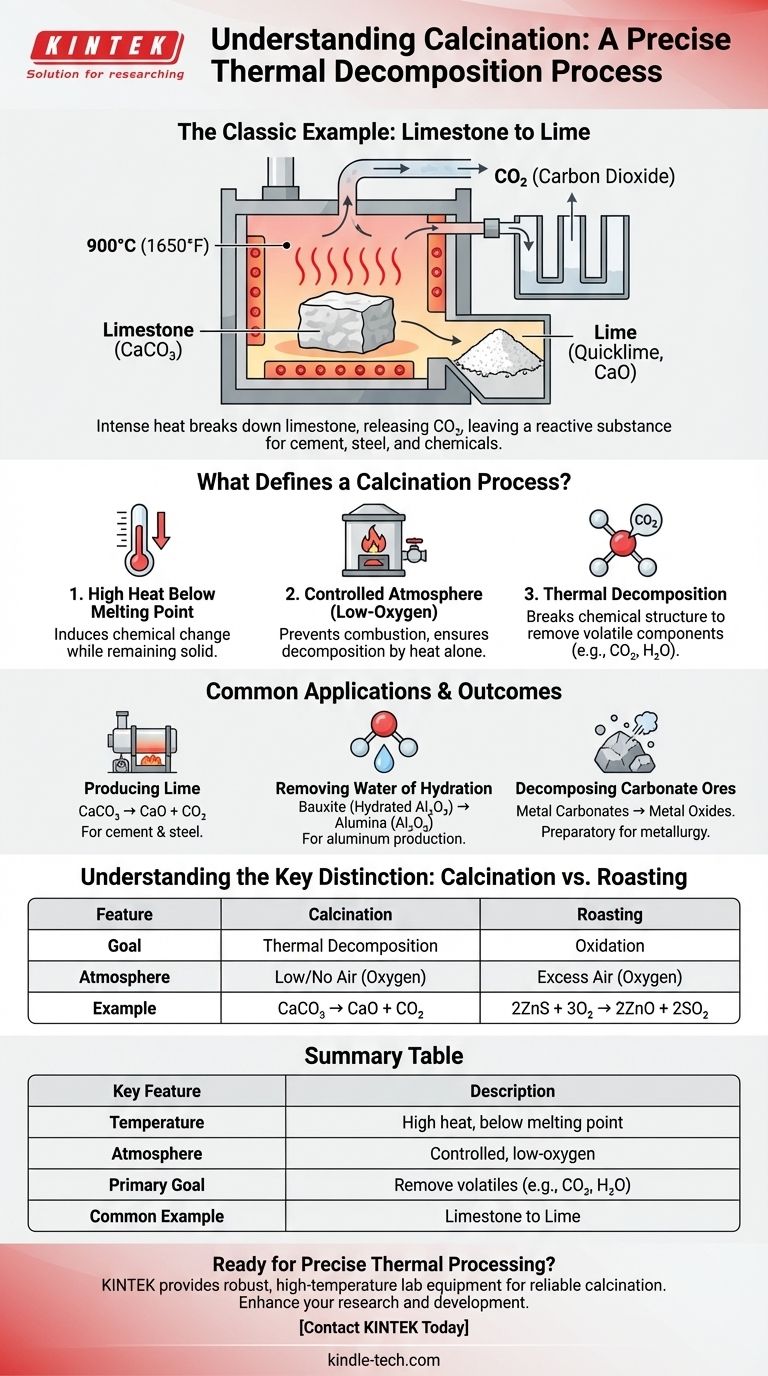
L'esempio classico di calcinazione è il riscaldamento del calcare (carbonato di calcio) per produrre calce (ossido di calcio). In questo processo, il calore intenso scompone il calcare, facendogli rilasciare anidride carbonica e lasciando dietro di sé una sostanza polverosa e più reattiva. Questo è un processo fondamentale utilizzato da secoli nella produzione di cemento e altri materiali industriali.
La calcinazione non è semplicemente riscaldamento; è un preciso processo di decomposizione termica. Utilizza alte temperature al di sotto del punto di fusione del materiale in un'atmosfera controllata e a basso contenuto di ossigeno per rimuovere componenti volatili come anidride carbonica o acqua.

Cosa definisce un processo di calcinazione?
Per identificare veramente la calcinazione, devi guardare oltre la semplice applicazione del calore. Tre condizioni specifiche definiscono il processo e lo separano da altri trattamenti termici come la torrefazione o l'essiccazione.
Il ruolo del calore elevato
La calcinazione comporta il riscaldamento di un materiale solido a una temperatura molto elevata. Fondamentalmente, questa temperatura è mantenuta al di sotto del punto di fusione del materiale.
L'obiettivo è indurre un cambiamento chimico o una decomposizione mentre il materiale rimane nel suo stato solido, spesso rendendolo fragile o poroso.
Un'atmosfera controllata
Il processo viene condotto in assenza o con una fornitura molto limitata di aria (ossigeno). Questa è una differenza chiave rispetto ad altri processi termici.
Limitando l'ossigeno, la calcinazione previene la combustione o un'ossidazione significativa. L'obiettivo primario è la decomposizione guidata dal solo calore, non dalla reazione con l'aria.
L'obiettivo: decomposizione termica
Lo scopo fondamentale della calcinazione è rompere la struttura chimica di una sostanza.
Questa decomposizione comporta la rimozione di un componente volatile dal solido. La parte che viene espulsa è tipicamente un gas, come l'anidride carbonica (CO2) dai carbonati o il vapore acqueo (H2O) dai minerali idrati.
Applicazioni e risultati comuni
Sebbene la produzione di calce sia il caso da manuale, la calcinazione è utilizzata in vari settori per trasformare i materiali.
Produzione di calce dal calcare
Questo è l'esempio più comune. Il calcare (CaCO₃) viene riscaldato a temperature intorno ai 900°C (1650°F). Si decompone in calce viva (CaO) e rilascia anidride carbonica.
Questa calce è un ingrediente cruciale nella produzione di cemento, acciaio e alcune sostanze chimiche.
Rimozione dell'acqua di idratazione
La calcinazione è ampiamente utilizzata per rimuovere l'acqua chimicamente legata dai minerali idrati.
Ad esempio, il minerale di bauxite, una forma idrata di ossido di alluminio, viene calcinato per eliminare l'acqua e produrre allumina pura (Al₂O₃), la principale materia prima per la produzione di alluminio metallico.
Decomposizione dei minerali carbonatici
Similmente al calcare, altri minerali carbonatici metallici vengono calcinati per convertirli nelle loro forme ossidate.
Questo è spesso un passaggio preparatorio in metallurgia, poiché gli ossidi metallici sono generalmente più facili da ridurre a metallo puro rispetto alle loro forme carbonatiche originali.
Comprendere le distinzioni chiave
Un punto comune di confusione è distinguere la calcinazione da un processo simile chiamato torrefazione. La distinzione è critica e risiede interamente nell'obiettivo e nell'atmosfera utilizzata.
Calcinazione vs. Torrefazione
La calcinazione mira alla decomposizione termica in assenza di aria. Pensala come "cuocere" un minerale per scomporlo. Un esempio è CaCO₃ → CaO + CO₂.
La torrefazione, al contrario, è il riscaldamento di un minerale in un eccesso di aria (ossigeno). L'obiettivo è l'ossidazione, spesso per convertire i minerali solfuri in ossidi. Un esempio è 2ZnS + 3O₂ → 2ZnO + 2SO₂.
Perché controllare l'atmosfera?
Limitare l'aria durante la calcinazione è essenziale per prevenire reazioni collaterali indesiderate. Se l'ossigeno fosse presente durante il riscaldamento del calcare, ad esempio, non cambierebbe fondamentalmente la reazione primaria, ma per altri materiali potrebbe portare a un'ossidazione indesiderata.
Il controllo dell'atmosfera assicura che la decomposizione termica sia la trasformazione dominante e intenzionale.
Come identificare un processo di calcinazione
Basandosi su questi principi, è possibile identificare facilmente se un processo è un esempio di calcinazione.
- Se il tuo obiettivo è decomporre un minerale carbonatico: Il riscaldamento di calcare, dolomite o altri carbonati per eliminare la CO₂ e formare un ossido è un esempio definitivo di calcinazione.
- Se il tuo obiettivo è rimuovere l'acqua chimicamente legata: Il riscaldamento di un minerale idrato come la bauxite o il gesso per produrre la sua forma anidra (priva di acqua) è un'altra applicazione primaria della calcinazione.
- Se la distinzione chiave è l'atmosfera: Un processo che comporta il riscaldamento di un solido al di sotto del suo punto di fusione in poca o nessuna aria per causare una scomposizione chimica è calcinazione.
Riconoscere queste condizioni ti permette di distinguere la calcinazione come uno strumento fondamentale dell'ingegneria chimica e dei materiali.
Tabella riassuntiva:
| Caratteristica chiave | Descrizione |
|---|---|
| Temperatura | Calore elevato, ma al di sotto del punto di fusione del materiale. |
| Atmosfera | Ambiente controllato, a basso o nullo contenuto di ossigeno. |
| Obiettivo primario | Decomposizione termica per rimuovere componenti volatili (es. CO₂, H₂O). |
| Esempio comune | Riscaldamento del calcare (CaCO₃) per produrre calce (CaO). |
Pronto a ottenere una lavorazione termica precisa nel tuo laboratorio?
La calcinazione è un processo fondamentale per trasformare i materiali, dalla decomposizione dei carbonati alla disidratazione dei minerali. KINTEK è specializzata nella fornitura di attrezzature da laboratorio robuste e ad alta temperatura, come forni avanzati con controllo preciso dell'atmosfera, di cui hai bisogno per eseguire questi processi in modo affidabile e sicuro.
Che tu sia nel campo della scienza dei materiali, della metallurgia o dell'ingegneria chimica, le nostre soluzioni sono progettate per soddisfare le rigorose esigenze della tua ricerca e sviluppo. Lasciaci aiutarti a migliorare le capacità del tuo laboratorio.
Contatta KINTEK oggi per discutere le tue specifiche esigenze di lavorazione termica e scoprire l'attrezzatura giusta per la tua applicazione.
Guida Visiva
Prodotti correlati
- Fornace a Pirolisi Continua Elettrica Rotante per Lavorazione Piccola Scala
- Impianto di pirolisi a forno rotante elettrico Macchina Calcinatore Piccolo Forno Rotante Forno Rotante
Domande frequenti
- Come vengono riscaldati i forni rotativi? Spiegazione dei metodi di riscaldamento diretto e indiretto
- Quali sono le caratteristiche delle modalità di movimento del letto a scorrimento, cedimento e rotolamento? Ottimizza il tuo processo rotativo
- Quali sono i principi di un forno rotante? Padroneggiare la meccanica della lavorazione ad alta temperatura
- Quali sono i diversi tipi di calcinatori? Una guida alla scelta dell'attrezzatura giusta per la lavorazione termica
- A quale temperatura avviene la pirolisi? Una guida per controllare la resa del tuo prodotto

