Alla base, la conversione della biomassa si basa su una serie di reazioni termochimiche controllate per scomporre la materia organica complessa. Processi come la gassificazione, la pirolisi e la combustione manipolano la temperatura e l'ossigeno per trasformare la biomassa in prodotti preziosi come il gas di sintesi (syngas), il bio-olio o il calore, guidati da reazioni fondamentali che coinvolgono carbonio, idrogeno e ossigeno.
La sfida centrale della conversione della biomassa non è semplicemente avviare reazioni chimiche, ma controllarle con precisione. Gestendo fattori come la temperatura e la quantità di ossigeno, possiamo orientare il processo a favore della creazione di combustibili e prodotti chimici preziosi rispetto alla semplice combustione in calore e anidride carbonica.

Le Principali Vie Termochimiche
Per comprendere la chimica, è necessario prima comprendere i metodi primari. La differenza chiave tra essi è la quantità di ossigeno fornita al processo, che determina i prodotti finali.
Combustione (Alto Ossigeno)
La combustione è l'ossidazione completa della biomassa in presenza di ossigeno in eccesso.
Il suo scopo primario è rilasciare la massima quantità di energia sotto forma di calore. Questo calore può quindi essere utilizzato per produrre vapore per la generazione di elettricità o per applicazioni di riscaldamento diretto. I prodotti principali sono anidride carbonica (CO₂) e acqua (H₂O).
Pirolisi (Nessun Ossigeno)
La pirolisi è la decomposizione termica della biomassa in completa assenza di ossigeno.
Invece di bruciare, la biomassa si scompone in tre prodotti principali: un liquido noto come bio-olio, un residuo solido chiamato biochar e una miscela gassosa nota come syngas.
Gassificazione (Ossigeno Limitato)
La gassificazione è un processo di ossidazione parziale che utilizza una quantità limitata e controllata di ossigeno o vapore.
È progettata per convertire la biomassa solida principalmente in una miscela di gas combustibile chiamata syngas, ricca di idrogeno (H₂) e monossido di carbonio (CO). Questo syngas è un intermedio versatile che può essere bruciato per generare elettricità o utilizzato come materia prima chimica.
Un'Analisi Approfondita della Chimica della Gassificazione
La chimica della gassificazione è un processo a più stadi in cui la combustione iniziale fornisce l'energia per le reazioni successive che producono il syngas desiderato. Le reazioni elencate di seguito spesso avvengono simultaneamente in diverse zone di un gassificatore.
Fase 1: Combustione Iniziale (Ossidazione)
Il processo inizia introducendo una piccola quantità di ossigeno, che avvia le reazioni di combustione. Queste sono esotermiche (rilasciano calore), fornendo le alte temperature necessarie per il resto del processo.
C + O₂ → CO₂(Combustione Completa)C + ½O₂ → CO(Combustione Parziale)H₂ + ½O₂ → H₂O(Combustione dell'Idrogeno)
Fase 2: Gassificazione Centrale (Riduzione)
Nell'ambiente ad alta temperatura e povero di ossigeno creato dalla combustione iniziale, la CO₂ calda e il vapore (H₂O) reagiscono con il carbonio rimanente (char). Queste sono le critiche reazioni endotermiche (assorbono calore) che producono syngas.
- Reazione di Boudouard:
C + CO₂ ↔ 2CO - Reazione Gas-Acqua:
C + H₂O ↔ CO + H₂
Queste due reazioni sono il cuore della conversione del carbonio solido in prezioso combustibile gassoso.
Fase 3: Reazioni Secondarie in Fase Gassosa
Una volta formato il syngas iniziale, avvengono ulteriori reazioni in fase gassosa che ne alterano la composizione finale. Il controllo di queste aiuta a ottimizzare il gas per l'uso previsto.
-
Reazione di Spostamento Gas-Acqua:
CO + H₂O ↔ H₂ + CO₂Questa reazione è cruciale per regolare il rapporto idrogeno-monossido di carbonio nel syngas finale. -
Reazioni di Metanazione:
C + 2H₂ ↔ CH₄CO + 3H₂ ↔ CH₄ + H₂OQueste reazioni producono metano (CH₄), che aumenta il potere calorifico del gas ma potrebbe essere indesiderabile se l'obiettivo è H₂ o CO puro.
Comprendere i Compromessi
La gestione efficace di un processo di conversione della biomassa è un atto di equilibrio. Le condizioni ideali dipendono interamente dal prodotto finale desiderato.
Il Dilemma dell'Ossigeno
La quantità di ossigeno è il parametro di controllo più critico. Troppo ossigeno porta alla combustione completa, rilasciando energia sotto forma di calore ma distruggendo il prezioso syngas. Troppo poco ossigeno non riuscirà a produrre abbastanza calore, bloccando le reazioni di gassificazione endotermiche.
Il Conflitto della Temperatura
Temperature più elevate (superiori a 800°C) favoriscono la produzione di idrogeno e monossido di carbonio tramite le reazioni di Boudouard e Gas-Acqua. Tuttavia, mantenere queste alte temperature richiede un maggiore apporto energetico o consuma più materia prima per la combustione.
Il Ruolo dell'Umidità e del Catrame
La biomassa non è carbonio puro. Il suo contenuto di umidità alimenta direttamente le reazioni Gas-Acqua e Spostamento Gas-Acqua, influenzando il rapporto H₂/CO. La conversione incompleta, specialmente a temperature più basse, può anche produrre idrocarburi complessi noti come catrami, che possono intasare le apparecchiature e rappresentano una significativa sfida operativa.
Fare la Scelta Giusta per il Tuo Obiettivo
Il percorso chimico ottimale dipende interamente da ciò che si vuole ottenere.
- Se il tuo obiettivo principale è generare direttamente calore o elettricità: La combustione completa è il percorso più semplice, massimizzando il rilascio immediato di energia.
- Se il tuo obiettivo principale è creare combustibili liquidi o materie prime chimiche: La gassificazione è superiore, in quanto produce un intermedio syngas versatile che può essere convertito cataliticamente in combustibili (tramite Fischer-Tropsch) o prodotti chimici come il metanolo.
- Se il tuo obiettivo principale è produrre biochar per l'amendamento del suolo: La pirolisi è il processo target, in quanto massimizza il residuo solido di char co-producendo bio-olio e gas.
Comprendendo queste vie chimiche fondamentali, puoi controllare efficacemente la trasformazione della biomassa grezza in energia e prodotti preziosi.
Tabella Riepilogativa:
| Processo | Livello di Ossigeno | Prodotti Primari | Applicazione Chiave |
|---|---|---|---|
| Combustione | Alto | Calore, CO₂, H₂O | Calore/elettricità diretta |
| Pirolisi | Nessuno | Bio-olio, Biochar, Syngas | Combustibili liquidi, amendamento del suolo |
| Gassificazione | Limitato | Syngas (H₂, CO) | Materie prime chimiche, elettricità |
Pronto a Ottimizzare il Tuo Processo di Conversione della Biomassa?
KINTEK è specializzata in attrezzature da laboratorio avanzate e materiali di consumo per la ricerca e lo sviluppo sulla biomassa. Che tu stia sviluppando catalizzatori, analizzando bio-olio o aumentando la scala delle reazioni di gassificazione, i nostri strumenti precisi ti aiutano a controllare parametri critici come temperatura e atmosfera. Lascia che i nostri esperti supportino il tuo percorso dalla biomassa grezza a preziosi prodotti energetici.
Contatta il nostro team oggi stesso per discutere le tue specifiche sfide di conversione della biomassa e scoprire l'attrezzatura giusta per il tuo laboratorio.
Guida Visiva
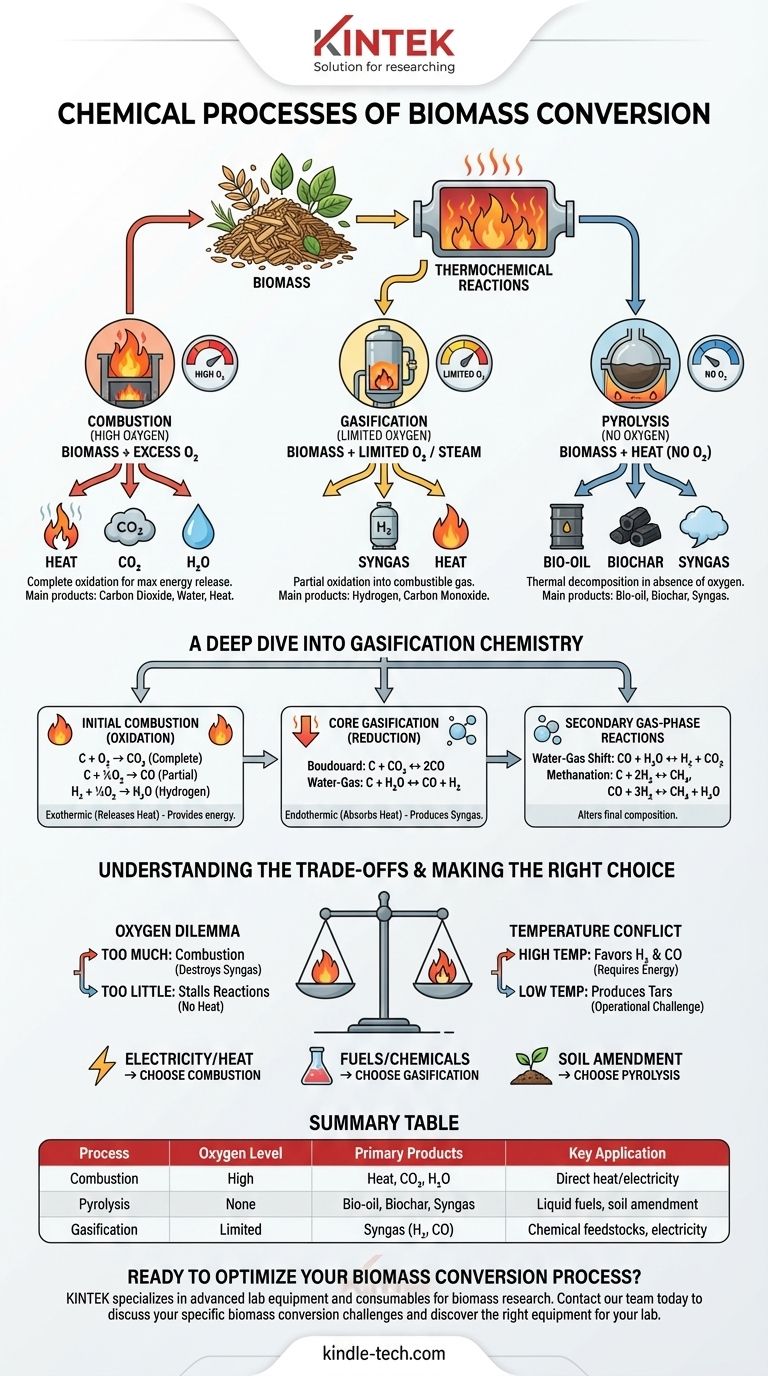
Prodotti correlati
- Fornace a Pirolisi per Biomassa Rotante Elettrica Piccola Fornace Rotante
- Reattori da laboratorio personalizzabili ad alta temperatura e alta pressione per diverse applicazioni scientifiche
- Mini reattore autoclave ad alta pressione in acciaio inossidabile per uso di laboratorio
- Reattore Autoclave da Laboratorio ad Alta Pressione per Sintesi Idrotermale
- Reattore Autoclave di Laboratorio ad Alta Pressione in Acciaio Inossidabile
Domande frequenti
- Come vengono riscaldati i forni rotativi? Spiegazione dei metodi di riscaldamento diretto e indiretto
- A quale temperatura avviene la pirolisi? Una guida per controllare la resa del tuo prodotto
- Quali sono le caratteristiche delle modalità di movimento del letto a scorrimento, cedimento e rotolamento? Ottimizza il tuo processo rotativo
- Quali sono i reattori per la pirolisi veloce? Scegliere il sistema giusto per la massima resa di bio-olio
- Quali sono le reazioni coinvolte nella pirolisi della biomassa? Sblocca la chimica per bio-prodotti su misura







