In sostanza, il cloruro di potassio (KCl) è utilizzato nell'elettrodo a calomelano per due ragioni fondamentali. In primo luogo, lo ione cloruro (Cl⁻) è un componente chiave nella reazione chimica che stabilisce la tensione stabile dell'elettrodo. In secondo luogo, i suoi ioni potassio (K⁺) e cloruro (Cl⁻) si muovono a velocità quasi identiche in soluzione, che è la caratteristica distintiva di un elettrolita ideale per ponte salino.
La duplice funzione del KCl è la chiave del successo dell'elettrodo a calomelano. Non è semplicemente un componente passivo; partecipa attivamente alla definizione del potenziale di riferimento e contemporaneamente previene errori di misurazione fungendo da ponte salino altamente efficace.

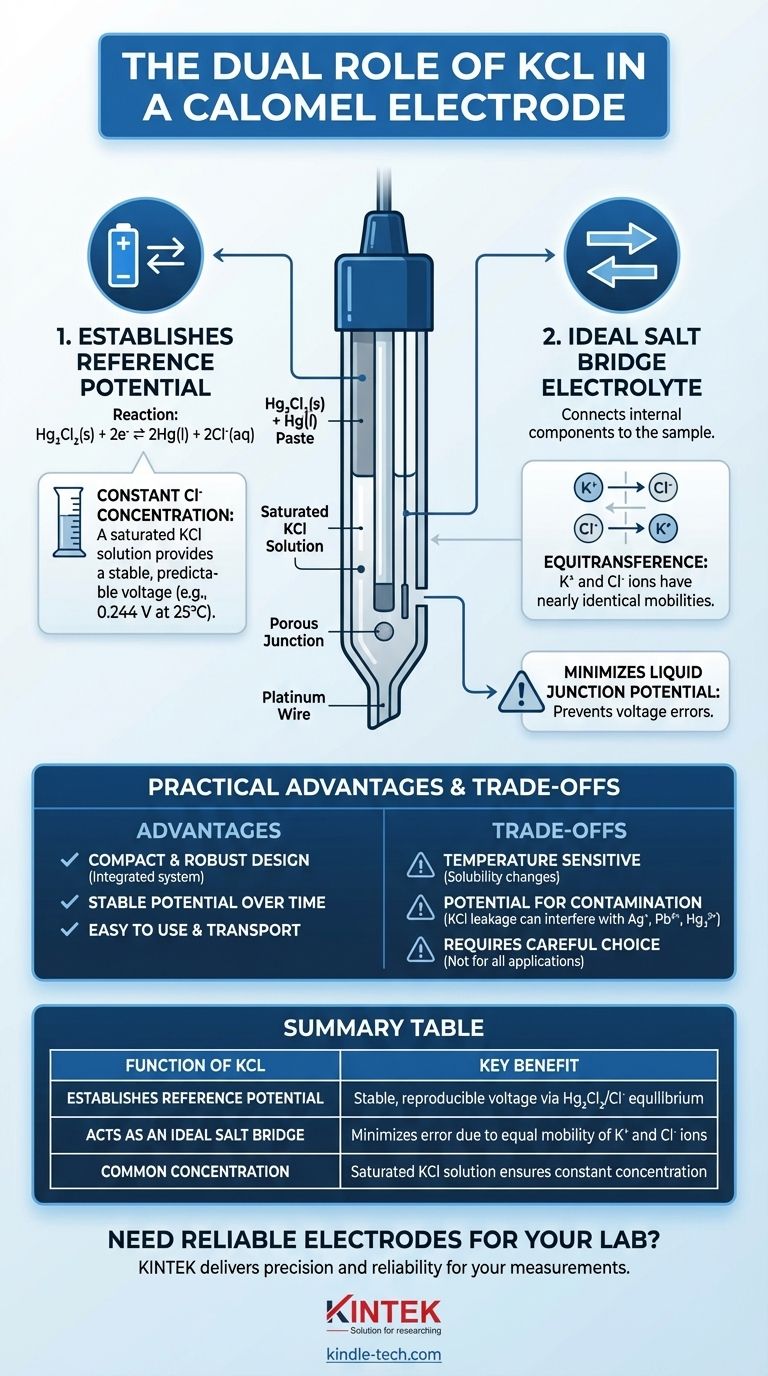
Il Doppio Ruolo del KCl nella Funzione dell'Elettrodo
La scelta del KCl è una decisione ingegneristica deliberata volta a creare un elettrodo di riferimento stabile, riproducibile e conveniente. Svolge due scopi distinti ma ugualmente importanti.
Stabilire il Potenziale di Riferimento
La tensione di un elettrodo a calomelano è generata da un equilibrio chimico specifico: Hg₂Cl₂(s) + 2e⁻ ⇌ 2Hg(l) + 2Cl⁻(aq).
Il potenziale di questa reazione dipende direttamente dalla concentrazione degli ioni cloruro (Cl⁻) nella soluzione. Riempendo l'elettrodo con una soluzione di KCl a concentrazione nota e costante, si stabilisce un potenziale di riferimento stabile e prevedibile.
Molto comunemente, si utilizza una soluzione di KCl satura. Ciò assicura che la concentrazione rimanga costante anche in caso di evaporazione di parte dell'acqua, fornendo una tensione altamente riproducibile che lo rende un punto di riferimento affidabile per le misurazioni elettrochimiche.
Funzionare come Ponte Salino Ideale
La soluzione di KCl funge anche da ponte salino, collegando i componenti interni dell'elettrodo di riferimento alla soluzione campione che si sta misurando.
Un ponte salino efficace richiede che i suoi ioni positivi e negativi migrino attraverso la soluzione a velocità quasi uguali. Questa proprietà è nota come equitrasferimento.
Se un ione si muove significativamente più velocemente dell'altro, si accumula una separazione di carica al confine tra le due soluzioni. Questo crea una tensione indesiderata nota come potenziale di giunzione liquida, che introduce un errore significativo nella misurazione.
Le mobilità degli ioni K⁺ e Cl⁻ sono quasi identiche, il che minimizza questo potenziale di giunzione e assicura l'accuratezza della misurazione.
Vantaggi Pratici e Compromessi
L'uso del KCl comporta notevoli vantaggi pratici, ma introduce anche considerazioni che ogni analista deve comprendere.
Perché il KCl è Conveniente
La natura integrata del KCl, che serve sia la reazione dell'elettrodo sia il ponte salino, consente un design compatto e robusto.
Un elettrodo a calomelano non richiede un ponte salino esterno separato. Ciò lo rende più facile da configurare, utilizzare e trasportare rispetto ad altri sistemi di riferimento. Il suo potenziale è inoltre noto per essere molto stabile nel tempo.
L'Impatto della Concentrazione
Il potenziale dell'elettrodo a calomelano dipende interamente dalla concentrazione di KCl. Sebbene la soluzione satura di KCl sia la più comune, per applicazioni specifiche vengono utilizzate anche altre concentrazioni come 1 M o 0,1 M.
L'uso di una soluzione satura è conveniente perché la concentrazione è autoregolante, ma significa anche che il potenziale dell'elettrodo è più sensibile alle variazioni di temperatura, poiché la solubilità del KCl cambia con la temperatura.
Potenziale di Contaminazione
Un compromesso critico è che la soluzione di riempimento dell'elettrodo può fuoriuscire lentamente nel campione attraverso la giunzione porosa.
Se la tua analisi coinvolge ioni che precipitano con il cloruro, come argento (Ag⁺), piombo (Pb²⁺) o mercurio (Hg₂²⁺), la fuoriuscita di KCl può causare interferenze e risultati imprecisi.
Fare la Scelta Giusta per il Tuo Obiettivo
Comprendere il ruolo del KCl ti aiuta a determinare quando un elettrodo a calomelano è lo strumento giusto per la tua specifica misurazione elettrochimica.
- Se la tua priorità principale è la riproducibilità e la facilità d'uso: un Elettrodo a Calomelano Saturato (SCE) è una scelta eccellente e classica, a condizione che il tuo campione sia privo di ioni interferenti e la temperatura sia stabile.
- Se la tua priorità principale è minimizzare la contaminazione da cloruro: devi utilizzare un sistema di riferimento diverso, come un elettrodo a mercurio-solfato mercurioso, che utilizza un elettrolita privo di cloruro.
- Se la tua priorità principale è la prestazione a temperature variabili: un elettrodo con una soluzione di KCl non satura (ad esempio 3 M) offre un potenziale più stabile rispetto alle variazioni di temperatura rispetto a una versione satura.
In definitiva, la scelta del KCl è fondamentale per la progettazione dell'elettrodo a calomelano, fornendo la base stabile necessaria per misurazioni accurate e affidabili.
Tabella Riassuntiva:
| Funzione del KCl | Vantaggio Chiave |
|---|---|
| Stabilisce il Potenziale di Riferimento | Fornisce una tensione stabile e riproducibile tramite l'equilibrio Hg₂Cl₂/Cl⁻. |
| Agisce come Ponte Salino Ideale | Minimizza l'errore di misurazione grazie alla mobilità quasi uguale degli ioni K⁺ e Cl⁻. |
| Concentrazione Comune | La soluzione di KCl satura assicura che la concentrazione rimanga costante, migliorando la riproducibilità. |
Hai bisogno di un elettrodo di riferimento affidabile per l'analisi elettrochimica del tuo laboratorio?
In KINTEK, comprendiamo che l'accuratezza delle tue misurazioni dipende da apparecchiature di laboratorio di alta qualità. La nostra gamma di elettrodi e materiali di consumo è progettata per fornire la precisione e l'affidabilità richieste dal tuo laboratorio.
Lascia che i nostri esperti ti aiutino a selezionare l'attrezzatura perfetta per la tua specifica applicazione. Contatta KINTEK oggi stesso per discutere le tue esigenze e assicurare il successo del tuo laboratorio!
Guida Visiva
Prodotti correlati
- Elettrodi di Riferimento Calomel Argento Cloruro Solfato di Mercurio per Uso di Laboratorio
- Elettrodo a disco d'oro
- Elettrodo a disco rotante in platino per applicazioni elettrochimiche
- Elettrodo Elettrochimico a Disco Metallico
- Elettrodo a foglio d'oro per elettrochimica Elettrodo d'oro
Domande frequenti
- Quale elettrodo viene utilizzato come riferimento di massa? Padroneggia la chiave per misurazioni elettrochimiche accurate
- Qual è la funzione di un elettrodo di riferimento? Padroneggia la precisione nella ricostruzione di reattori a tre elettrodi
- Quale elettrodo viene utilizzato come elettrodo di riferimento per la misurazione dei potenziali di semicella? Comprendere lo standard universale
- Quale elettrodo viene utilizzato come riferimento? Una guida per misurazioni elettrochimiche accurate
- Qual è lo scopo dell'elettrodo di riferimento? Ottenere misurazioni elettrochimiche stabili e accurate











