Un esempio classico di elettrodeposizione è il processo di doratura dei gioielli. In questa applicazione, una corrente elettrica viene utilizzata per spostare gli ioni d'oro da una soluzione sulla superficie di un metallo meno costoso, creando uno strato sottile, durevole e lucido d'oro. Questa stessa tecnica fondamentale viene utilizzata per tutto, dalla cromatura dei paraurti delle auto alla fabbricazione di minuscoli cablaggi in rame nei chip dei computer.
L'elettrodeposizione è essenzialmente un processo di verniciatura guidato elettricamente. Utilizza una corrente elettrica controllata per trasferire con precisione ioni metallici attraverso una soluzione liquida (un elettrolita) e depositarli come un film solido sottile su un oggetto conduttivo.

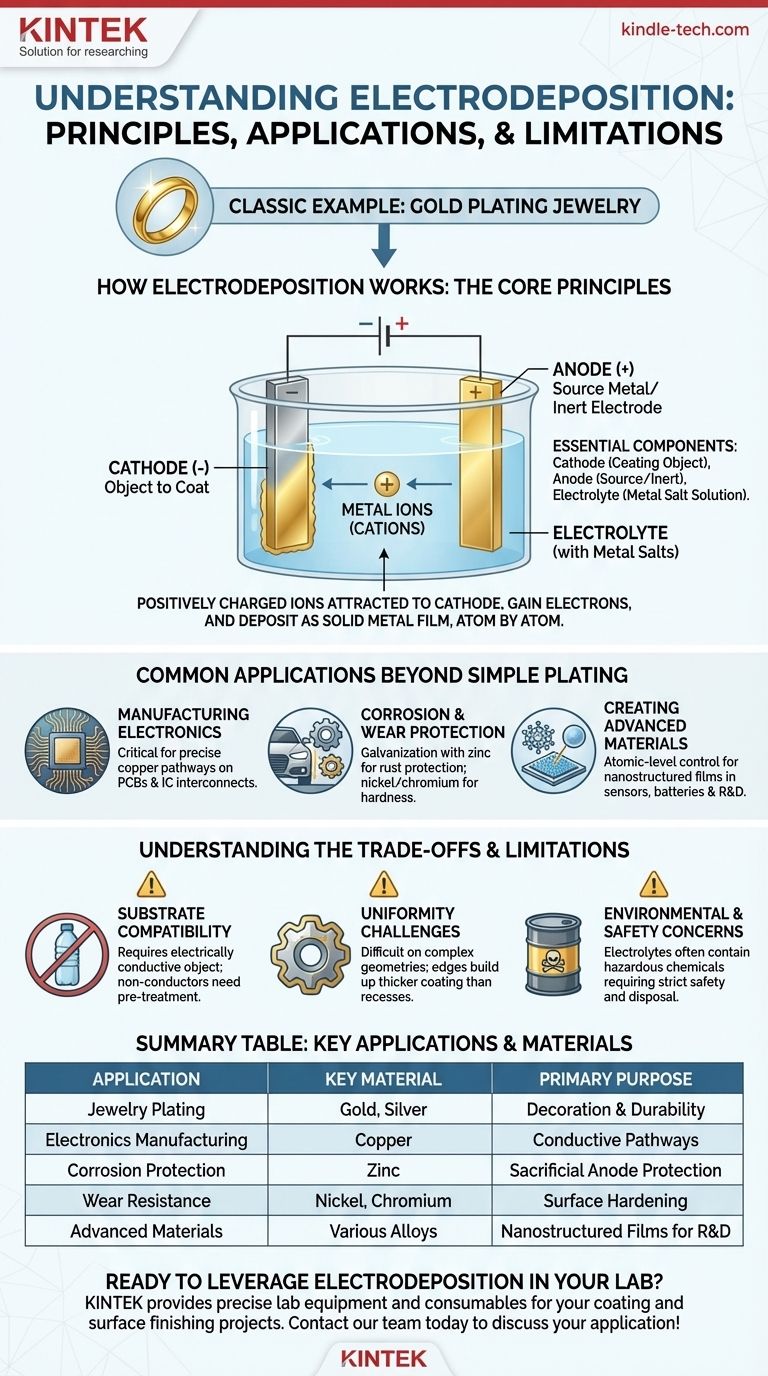
Come funziona l'elettrodeposizione: i principi fondamentali
Per comprendere l'elettrodeposizione, è necessario visualizzare tre componenti chiave che lavorano insieme in una cella elettrochimica.
I componenti essenziali
L'allestimento è costituito da due elettrodi immersi in un liquido speciale.
- Il Catodo: Questo è l'oggetto che si desidera rivestire. È collegato al terminale negativo di una fonte di alimentazione.
- L'Anodo: Questa è la fonte di metallo (o un elettrodo inerte). È collegato al terminale positivo della fonte di alimentazione.
- L'Elettrolita: Questa è una soluzione, spesso contenente sali disciolti del metallo che si desidera depositare (ad esempio, sali d'oro per la doratura).
La reazione elettrochimica
Quando l'alimentazione viene accesa, si stabilisce un campo elettrico tra i due elettrodi. Questo avvia una reazione chimica controllata.
Gli ioni metallici con carica positiva (cationi) che galleggiano nell'elettrolita sono attratti dal catodo carico negativamente.
Costruire lo strato di rivestimento strato per strato
Quando gli ioni raggiungono il catodo, acquisiscono elettroni e vengono "ridotti" al loro stato metallico solido, depositandosi sulla superficie.
Questo processo costruisce il rivestimento un livello atomico alla volta, risultando in un film altamente uniforme e ben aderente. Nel frattempo, l'anodo può dissolversi per reintegrare gli ioni metallici nella soluzione, mantenendo il processo.
Applicazioni comuni oltre la semplice placcatura
Sebbene il rivestimento decorativo sia un esempio comune, il vero potere dell'elettrodeposizione risiede nella sua precisione e versatilità per le applicazioni industriali e tecnologiche.
Produzione di elettronica
L'elettrodeposizione è fondamentale per creare gli intricati percorsi di rame sui circuiti stampati (PCB) e gli interconnessioni all'interno dei circuiti integrati. La sua precisione consente la fabbricazione di linee conduttive microscopiche.
Protezione dalla corrosione e dall'usura
Un processo chiamato galvanizzazione utilizza l'elettrodeposizione per rivestire l'acciaio con uno strato di zinco. Lo strato di zinco si corrode preferenzialmente, sacrificandosi per proteggere l'acciaio sottostante dalla ruggine. I rivestimenti in nichel e cromo sono utilizzati anche per migliorare la durezza e la resistenza all'usura sulle parti industriali.
Creazione di materiali avanzati
Poiché offre un controllo a livello atomico, l'elettrodeposizione è utilizzata nella ricerca e nella produzione high-tech per creare film nanostrutturati. Questi materiali hanno proprietà uniche e sono utilizzati in sensori, catalizzatori e batterie avanzate.
Comprendere i compromessi e i limiti
Sebbene potente, l'elettrodeposizione non è una soluzione universale. Comprendere i suoi limiti è fondamentale per applicarla efficacemente.
Compatibilità del substrato
Il requisito principale è che l'oggetto da placcare (il substrato) debba essere elettricamente conduttivo. La placcatura su plastica, ceramica o altri isolanti richiede un complesso processo di pre-trattamento per applicare prima un sottile strato di semina conduttivo.
Sfide di uniformità
Ottenere un rivestimento perfettamente uniforme su oggetti con geometrie complesse può essere difficile. Le aree ad alta densità di corrente, come angoli acuti e bordi, tendono ad accumulare un rivestimento più spesso rispetto alle aree incassate o ai fori.
Preoccupazioni ambientali e di sicurezza
I bagni elettrolitici utilizzati nella galvanica spesso contengono sostanze chimiche acide, alcaline o tossiche (come il cianuro in alcuni processi). Questi materiali richiedono rigorosi protocolli di sicurezza per la manipolazione e procedure ecologicamente valide per lo smaltimento.
Fare la scelta giusta per il tuo obiettivo
Il motivo per cui si utilizza l'elettrodeposizione determinerà il materiale e i parametri di processo su cui ci si dovrebbe concentrare.
- Se il tuo obiettivo principale è l'estetica o la decorazione: Dai priorità a materiali come oro, argento, rodio o cromo per il loro aspetto e la loro durata sui beni di consumo.
- Se il tuo obiettivo principale è l'ingegneria e la protezione: Considera rivestimenti funzionali come zinco per la resistenza alla corrosione, nichel per la resistenza all'usura o rame per la conduttività.
- Se il tuo obiettivo principale è la ricerca avanzata o l'elettronica: Esplora il controllo preciso dell'elettrodeposizione per creare film legati o nanostrutture con specifiche proprietà catalitiche o elettriche.
Comprendendo l'elettrodeposizione come un metodo di rivestimento controllato e guidato elettricamente, puoi sfruttare efficacemente la sua potenza in innumerevoli applicazioni industriali e scientifiche.
Tabella riassuntiva:
| Applicazione | Materiale chiave | Scopo principale |
|---|---|---|
| Placcatura di gioielli | Oro, Argento | Decorazione e durata |
| Produzione di elettronica | Rame | Percorsi conduttivi |
| Protezione dalla corrosione (Galvanizzazione) | Zinco | Protezione come anodo sacrificale |
| Resistenza all'usura | Nichel, Cromo | Indurimento superficiale |
| Materiali avanzati | Vari leghe | Film nanostrutturati per R&S |
Pronto a sfruttare l'elettrodeposizione nel tuo laboratorio? KINTEK è specializzata nel fornire le attrezzature da laboratorio e i materiali di consumo precisi necessari per i tuoi progetti di rivestimento e finitura superficiale. Sia che tu stia sviluppando nuovi materiali o aumentando un processo di produzione, la nostra esperienza può aiutarti a ottenere risultati superiori. Contatta il nostro team oggi stesso per discutere le tue specifiche esigenze applicative!
Guida Visiva
Prodotti correlati
- Crogiolo in rame privo di ossigeno per rivestimento a evaporazione a fascio elettronico e barchetta di evaporazione
- Materiale per lucidatura elettrodi per esperimenti elettrochimici
- Supporto per elettrodi per esperimenti elettrochimici
- Cella Elettrochimica Elettrolitica a Diffusione di Gas Cella di Reazione a Flusso Liquido
- Elettrodo Elettrochimico a Disco Metallico
Domande frequenti
- A cosa serve l'evaporazione a fascio di elettroni? Rivestimenti di precisione per ottica, aerospaziale ed elettronica
- Cos'è l'evaporazione a fascio di elettroni? Ottenere deposizione di film sottili ad alta purezza per il tuo laboratorio
- Qual è la tensione dell'evaporazione a fascio di elettroni? Ottenere un deposito di film sottili preciso
- Qual è il tasso di deposizione dell'evaporazione a fascio elettronico? Controlla la qualità e la velocità del film sottile
- Quali sono le applicazioni dei fasci di elettroni? Dall'imaging su scala nanometrica alla produzione industriale



















