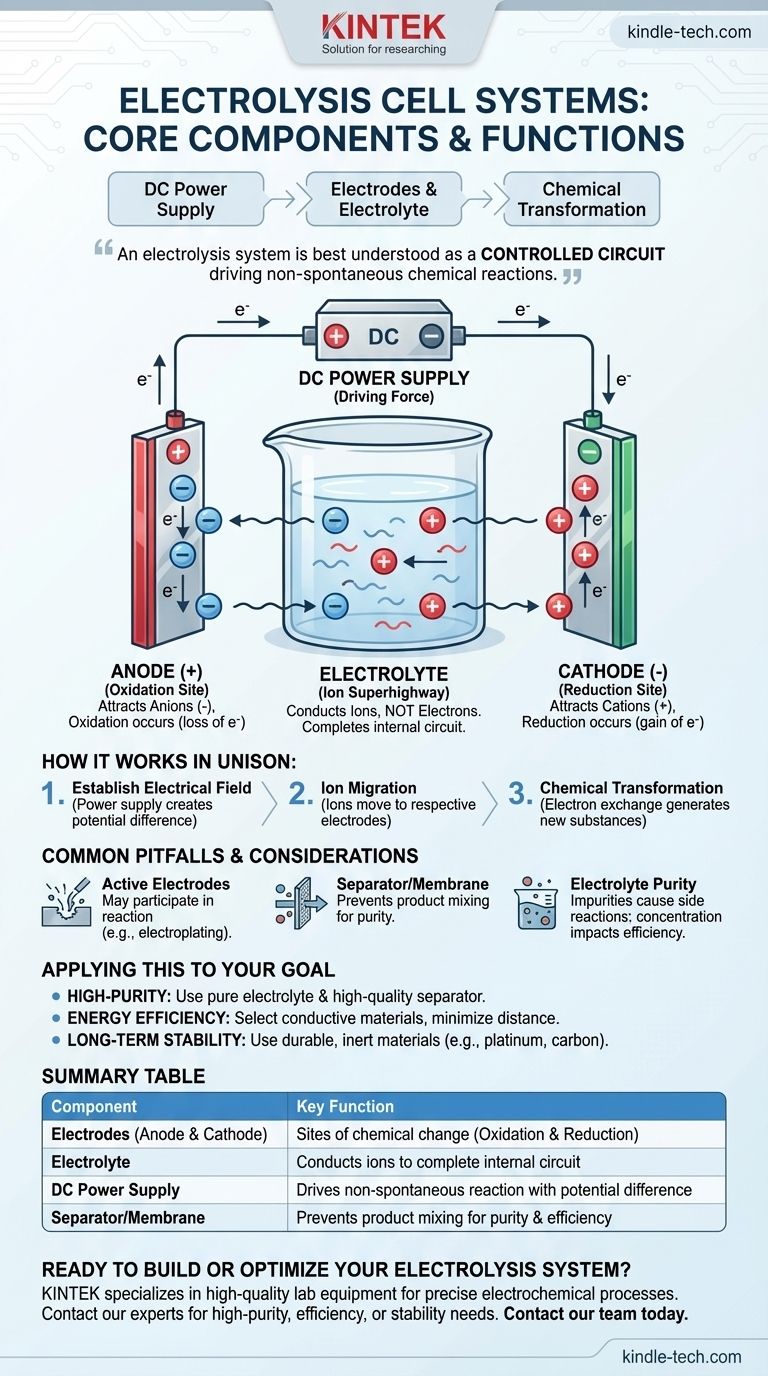
Al suo centro, un sistema a cella elettrolitica è composto da tre elementi essenziali: due elettrodi (un anodo e un catodo), un elettrolita contenente ioni e un alimentatore CC esterno. Questi elementi lavorano all'unisono per utilizzare l'energia elettrica per forzare una reazione chimica che non avverrebbe spontaneamente.
Un sistema di elettrolisi è meglio compreso non come una raccolta di parti, ma come un circuito controllato. L'alimentatore crea un potenziale elettrico, spingendo gli ioni attraverso l'elettrolita verso gli elettrodi, dove subiscono trasformazioni chimiche.

I componenti principali e i loro ruoli
Per comprendere come funziona l'elettrolisi, devi prima capire la funzione specifica di ciascun componente primario. Ognuno svolge un ruolo indispensabile e distinto nel processo.
Gli elettrodi: siti di cambiamento chimico
L'anodo e il catodo sono materiali conduttivi, tipicamente metalli o grafite, che fungono da interfaccia fisica tra il circuito esterno e l'elettrolita.
L'anodo è l'elettrodo positivo. Attrae ioni con carica negativa (anioni) dall'elettrolita. Sulla superficie dell'anodo, questi ioni perdono elettroni in un processo chiamato ossidazione.
Il catodo è l'elettrodo negativo. Attrae ioni con carica positiva (cationi). Qui, gli ioni acquistano elettroni in un processo chiamato riduzione.
L'elettrolita: l'autostrada ionica
L'elettrolita è una sostanza contenente ioni in movimento libero, il che lo rende elettricamente conduttivo. Spesso è una soluzione di un acido, una base o un sale disciolto in acqua.
Il suo unico scopo è condurre ioni, non elettroni. Il movimento di questi ioni tra gli elettrodi completa il circuito elettrico all'interno della cella, consentendo alla reazione di sostenersi.
L'alimentatore CC: la forza motrice
Questo è il motore esterno del sistema, spesso una batteria o un raddrizzatore. Guida la reazione non spontanea creando una differenza di potenziale elettrico attraverso gli elettrodi.
L'alimentatore pompa elettroni nel catodo, rendendolo negativo, e li rimuove dall'anodo, rendendolo positivo. Fondamentalmente, deve essere una fonte di corrente continua (CC) per mantenere questa polarità fissa.
Come funziona il sistema all'unisono
I componenti non sono indipendenti; formano un sistema integrato in cui la funzione di ogni parte abilita la successiva.
1. Stabilire il campo elettrico
Il processo inizia quando l'alimentatore viene acceso. Stabilisce immediatamente una carica positiva sull'anodo e una carica negativa sul catodo.
2. Migrazione ionica
Questo potenziale elettrico esercita una forza sugli ioni all'interno dell'elettrolita. I cationi con carica positiva sono attratti verso il catodo negativo, mentre gli anioni con carica negativa sono attratti verso l'anodo positivo.
3. La trasformazione chimica
Quando gli ioni raggiungono i rispettivi elettrodi, avviene lo scambio di elettroni. La sostanza viene scomposta mentre si formano nuovi composti o elementi sulle superfici degli elettrodi, come la generazione di gas idrogeno al catodo e gas ossigeno all'anodo durante l'elettrolisi dell'acqua.
Errori comuni e considerazioni
Una comprensione funzionale richiede il riconoscimento dei fattori pratici che influenzano il risultato e l'efficienza del processo.
Il materiale dell'elettrodo non è sempre inerte
Sebbene molti sistemi utilizzino elettrodi inerti (come platino o carbonio) che facilitano solo la reazione, alcune applicazioni utilizzano elettrodi attivi. Questi elettrodi partecipano alla reazione, dissolvendosi o venendo rivestiti di metallo, come si vede nella galvanostegia o nella raffinazione.
Il separatore è spesso necessario
In molte applicazioni industriali, un separatore o membrana viene posizionato tra l'anodo e il catodo. Questa barriera fisica consente il passaggio degli ioni ma impedisce ai prodotti appena formati di mescolarsi e reagire tra loro, il che ridurrebbe la purezza e l'efficienza.
La purezza e la concentrazione dell'elettrolita sono importanti
L'efficienza della cella è direttamente collegata alla capacità dell'elettrolita di condurre ioni. Le impurità possono causare reazioni secondarie indesiderate, mentre una concentrazione errata può ostacolare il flusso ionico e rallentare l'intero processo.
Applicare questo al tuo obiettivo
La tua progettazione e il tuo focus operativo dipenderanno interamente dal risultato desiderato dell'elettrolisi.
- Se il tuo obiettivo principale è ottenere prodotti di elevata purezza: Dai la priorità a una membrana separatrice di alta qualità e a un elettrolita puro per prevenire la contaminazione incrociata e le reazioni secondarie.
- Se il tuo obiettivo principale è l'efficienza energetica: Seleziona materiali per elettrodi altamente conduttivi e riduci al minimo la distanza fisica tra loro per diminuire la resistenza elettrica.
- Se il tuo obiettivo principale è la stabilità a lungo termine: Utilizza materiali per elettrodi durevoli e inerti che resistano alla corrosione da parte dell'elettrolita e dei prodotti di reazione.
Comprendendo come interagiscono questi componenti principali, puoi manipolare le reazioni chimiche con precisione e controllo.
Tabella riassuntiva:
| Componente | Funzione chiave |
|---|---|
| Elettrodi (Anodo e Catodo) | Siti di cambiamento chimico (Ossidazione e Riduzione) |
| Elettrolita | Conduce ioni per completare il circuito elettrico interno |
| Alimentatore CC | Guida la reazione non spontanea creando una differenza di potenziale |
| Separatore/Membrana (Comune) | Impedisce la miscelazione dei prodotti, aumentando purezza ed efficienza |
Pronto a costruire o ottimizzare il tuo sistema di elettrolisi? KINTEK è specializzata nella fornitura di attrezzature da laboratorio e materiali di consumo di alta qualità per processi elettrochimici precisi. Che il tuo obiettivo sia la generazione di prodotti di elevata purezza, l'efficienza energetica o la stabilità a lungo termine, i nostri esperti possono aiutarti a selezionare i componenti giusti. Contatta il nostro team oggi stesso per discutere le esigenze specifiche del tuo laboratorio!
Guida Visiva
Prodotti correlati
- Celle Elettrolitiche PEM Personalizzabili per Diverse Applicazioni di Ricerca
- Cella Elettrochimica per Elettrolisi Spettrale a Strato Sottile
- Cella Elettrochimica Elettrolitica a Diffusione di Gas Cella di Reazione a Flusso Liquido
- Cella Elettrolitica Elettrochimica a Cinque Porte
- Cella Elettrochimica Elettrolitica al Quarzo per Esperimenti Elettrochimici
Domande frequenti
- Qual è la procedura corretta per spegnere l'esperimento dopo l'elettrolisi? Una guida alla sicurezza passo-passo
- Qual è la procedura di conservazione corretta per una cella elettrolitica e i suoi componenti? Una guida passo-passo per preservare l'accuratezza
- Quali sono le configurazioni di apertura per le versioni non sigillate e sigillate della cella di elettrolisi? Ottimizza la tua configurazione elettrochimica
- Come devono essere pulite regolarmente la cella elettrolitica e i suoi elettrodi per la manutenzione? Una guida per risultati affidabili
- Qual è la procedura di pulizia immediata post-utilizzo per una cella elettrolitica? Prevenire l'accumulo di residui per risultati accurati



















