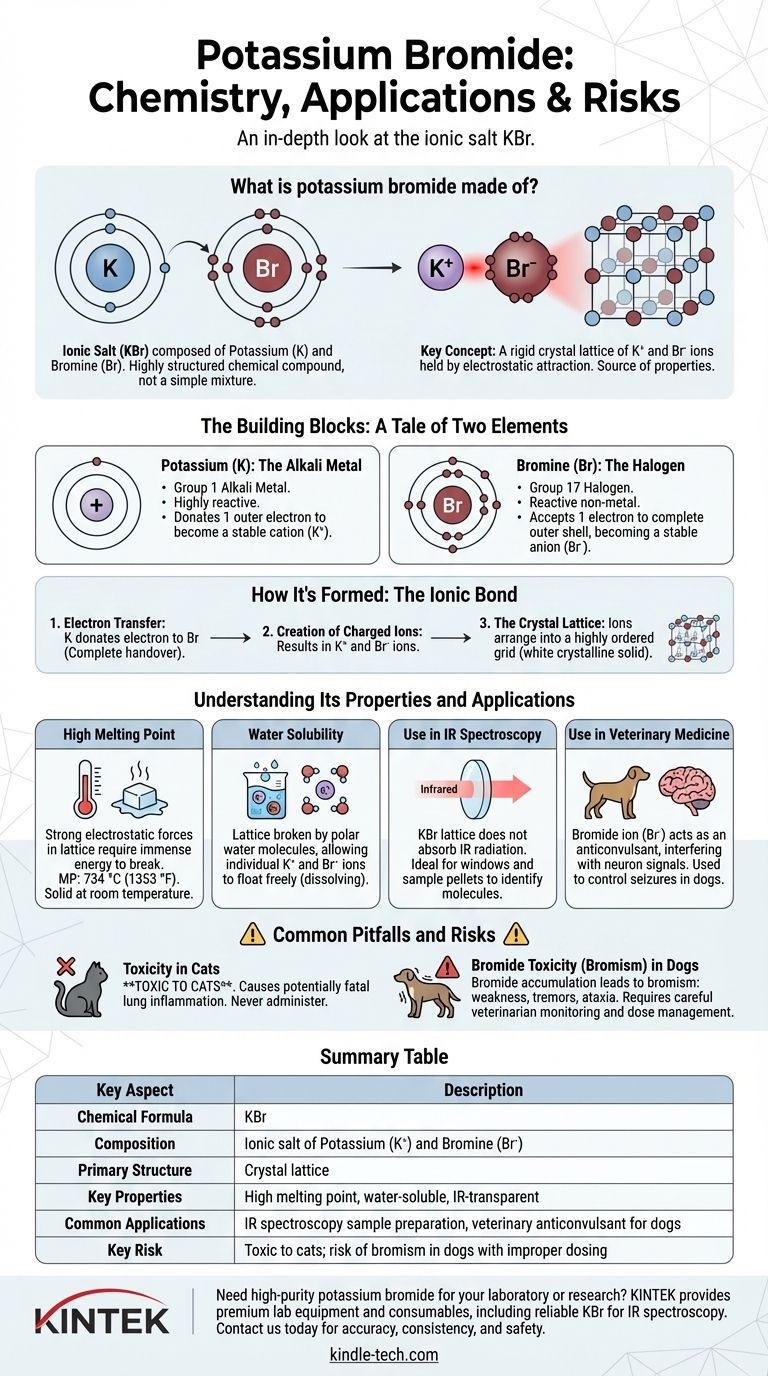
In breve, il bromuro di potassio è un sale ionico composto dagli elementi potassio e bromo. Non è una semplice miscela ma un composto chimico altamente strutturato con la formula KBr. L'atomo di potassio dona un elettrone all'atomo di bromo, creando particelle cariche (ioni) che sono tenute insieme da una forte attrazione elettrostatica.
La chiave per comprendere il bromuro di potassio è vederlo non come una collezione di atomi, ma come un reticolo cristallino rigido di ioni potassio caricati positivamente e ioni bromuro caricati negativamente. Questa struttura ionica è la fonte delle sue proprietà e applicazioni più importanti.

I blocchi costitutivi: una storia di due elementi
L'esistenza del bromuro di potassio è una conseguenza diretta delle proprietà chimiche fondamentali dei suoi due elementi costitutivi. Ciascuno ha un forte "desiderio" di raggiungere una configurazione elettronica più stabile.
Potassio (K): il metallo alcalino
Il potassio è un metallo morbido, altamente reattivo, che si trova nel Gruppo 1 della tavola periodica. La sua caratteristica distintiva è avere un singolo elettrone nel suo guscio più esterno.
È molto più stabile energeticamente se cede questo elettrone solitario. In questo modo, diventa uno ione caricato positivamente (K⁺).
Bromo (Br): l'alogeno
Il bromo è un non-metallo reattivo del Gruppo 17, gli alogeni. La sua caratteristica distintiva è avere sette elettroni nel suo guscio esterno, solo uno in meno rispetto a un set completo e stabile di otto.
Accetta prontamente un elettrone per completare questo guscio, diventando uno ione caricato negativamente (Br⁻), noto come ione bromuro.
Come si forma: il legame ionico
La formazione del bromuro di potassio è un classico esempio di legame ionico, che è definito dal trasferimento, non dalla condivisione, di elettroni.
Il trasferimento di elettroni
Quando il metallo potassio e il bromo reagiscono, ogni atomo di potassio dona il suo singolo elettrone esterno a un atomo di bromo. Questo non è una condivisione delicata ma un completo passaggio di mano.
Creazione di ioni carichi
Questo trasferimento di elettroni produce due particelle stabili, ma ora cariche: il catione potassio (K⁺) e l'anione bromuro (Br⁻). Poiché cariche opposte si attraggono, sono potentemente attratte l'una dall'altra.
Il reticolo cristallino
Questi ioni positivi e negativi non formano semplici coppie. Invece, si dispongono in una griglia tridimensionale altamente ordinata e ripetitiva chiamata reticolo cristallino. Questa struttura forte e rigida è ciò che rende il bromuro di potassio un solido cristallino bianco a temperatura ambiente.
Comprendere le sue proprietà e applicazioni
La natura ionica del bromuro di potassio spiega direttamente il suo comportamento fisico e chimico, che a sua volta ne determina gli usi.
Alto punto di fusione
Le potenti forze elettrostatiche che tengono insieme gli ioni K⁺ e Br⁻ nel reticolo cristallino richiedono un'enorme quantità di energia per essere spezzate. Questo è il motivo per cui il KBr è un solido con un alto punto di fusione di 734 °C (1353 °F).
Solubilità in acqua
Sebbene il reticolo sia forte, può essere scomposto da molecole polari come l'acqua. Le molecole d'acqua circondano i singoli ioni K⁺ e Br⁻, neutralizzando la loro carica e permettendo loro di galleggiare liberamente, cosa che percepiamo come la dissoluzione del sale.
Uso nella spettroscopia IR
Il reticolo cristallino di KBr non assorbe la radiazione infrarossa. Questa trasparenza lo rende un materiale ideale per la creazione di finestre e pastiglie per campioni utilizzate nella spettroscopia IR, una tecnica che aiuta i chimici a identificare le molecole.
Uso in medicina veterinaria
Lo ione bromuro (Br⁻) può agire come anticonvulsivante interferendo con il trasporto degli ioni cloruro nei neuroni del sistema nervoso centrale. Per questo motivo, il KBr è utilizzato in medicina veterinaria per controllare le crisi epilettiche nei cani.
Trappole e rischi comuni
Sebbene utile, il bromuro di potassio non è privo di rischi, che sono fondamentali da comprendere nelle sue applicazioni pratiche.
Tossicità nei gatti
Il rischio principale è nell'uso veterinario. Il bromuro di potassio è tossico per i gatti, causando una condizione polmonare infiammatoria potenzialmente fatale. Non dovrebbe mai essere somministrato a loro.
Tossicità da bromuro (Bromismo) nei cani
Anche nei cani, dove viene usato terapeuticamente, lo ione bromuro può accumularsi nel corpo nel tempo. Se i livelli diventano troppo alti, può portare a una condizione chiamata bromismo, con sintomi come debolezza, tremori e atassia. Questo richiede un'attenta gestione della dose e un monitoraggio da parte di un veterinario.
Come applicare questa conoscenza
La tua prospettiva sul bromuro di potassio dipenderà interamente dal tuo obiettivo.
- Se il tuo focus principale è la chimica: Vedilo come l'esempio per eccellenza di un legame ionico formato tra un metallo alcalino del Gruppo 1 e un alogeno del Gruppo 17.
- Se il tuo focus principale è l'analisi di laboratorio: Riconosci che la sua trasparenza IR e la capacità di essere pressato in una pastiglia solida sono le proprietà chiave che lo rendono inestimabile per la preparazione dei campioni.
- Se il tuo focus principale è la salute veterinaria: Comprendi che il suo effetto terapeutico deriva dallo ione bromuro, ma questo è inseparabile dal grave rischio di tossicità, specialmente nei gatti.
In definitiva, sapere che il KBr è costruito da ioni trasferiti tra un metallo e un non-metallo è la base per comprendere ogni suo uso e limitazione.
Tabella riassuntiva:
| Aspetto chiave | Descrizione |
|---|---|
| Formula chimica | KBr |
| Composizione | Sale ionico di potassio (K⁺) e bromo (Br⁻) |
| Struttura primaria | Reticolo cristallino |
| Proprietà chiave | Alto punto di fusione, solubile in acqua, trasparente all'IR |
| Applicazioni comuni | Preparazione di campioni per spettroscopia IR, anticonvulsivante veterinario per cani |
| Rischio chiave | Tossico per i gatti; rischio di bromismo nei cani con dosaggio improprio |
Hai bisogno di bromuro di potassio ad alta purezza per il tuo laboratorio o la tua ricerca? KINTEK è specializzata nella fornitura di attrezzature e materiali di consumo da laboratorio di alta qualità, incluso KBr affidabile per la spettroscopia IR e altre applicazioni. I nostri prodotti garantiscono precisione, coerenza e sicurezza per il tuo lavoro. Contattaci oggi per scoprire come possiamo supportare le tue esigenze di laboratorio con i materiali e l'esperienza giusti.
Guida Visiva
Prodotti correlati
- Elettrodi di Riferimento Calomel Argento Cloruro Solfato di Mercurio per Uso di Laboratorio
- Materiali diamantati drogati con boro tramite CVD
- Bagno d'acqua per cella elettrochimica elettrolitica multifunzionale a strato singolo e doppio
- Elettrodo di riferimento al solfato di rame per uso di laboratorio
- Presse Idraulica Automatica da Laboratorio per Pastiglie XRF & KBR
Domande frequenti
- Qual è la manutenzione raccomandata per la soluzione di riempimento di un elettrodo di riferimento? Una Guida per Letture Stabili e Accurate
- Qual è l'elettrodo di riferimento nella potenziometria? La chiave per misurazioni stabili e accurate
- Qual è lo scopo dell'elettrodo di riferimento? Ottenere misurazioni elettrochimiche stabili e accurate
- Quale elettrodo viene utilizzato come riferimento di massa? Padroneggia la chiave per misurazioni elettrochimiche accurate
- Quale elettrodo viene utilizzato come elettrodo di riferimento per la misurazione dei potenziali di semicella? Comprendere lo standard universale



















