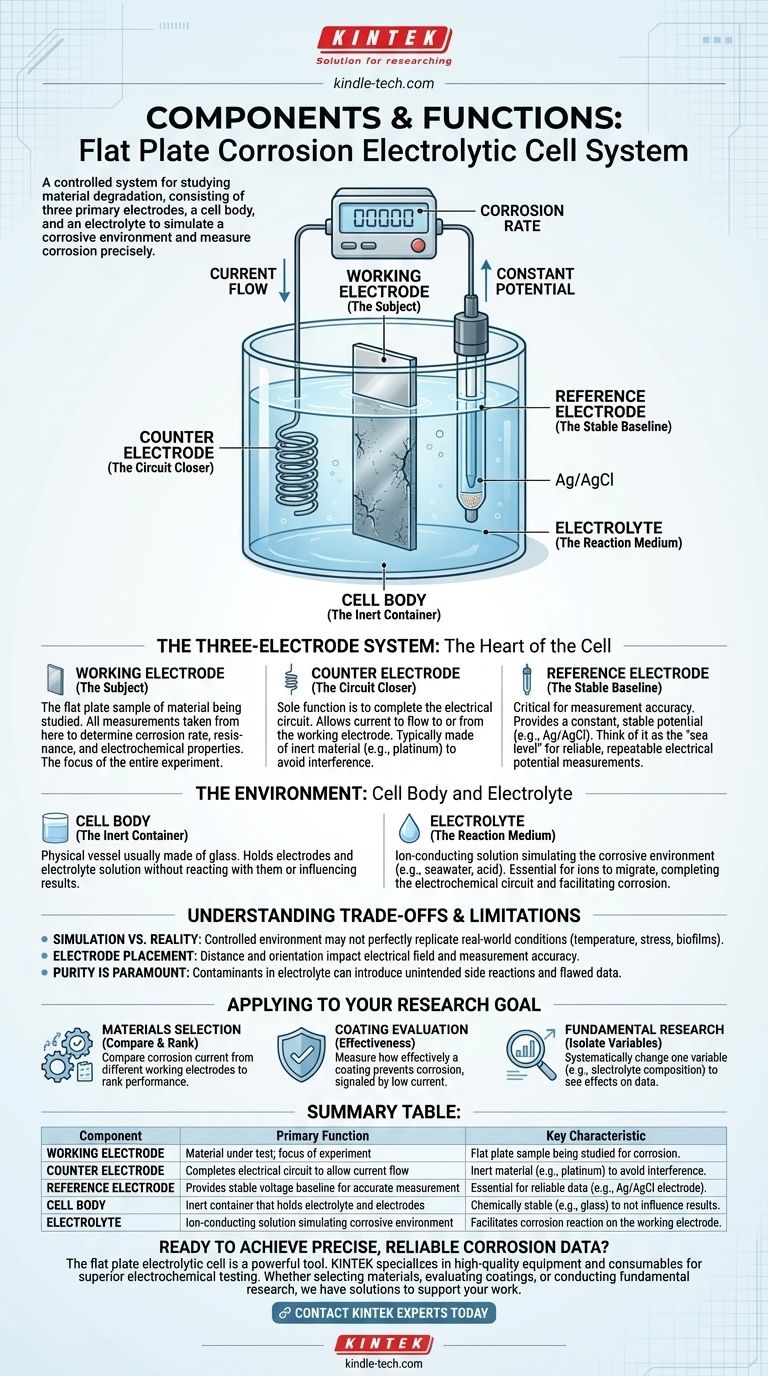
In sintesi, una cella elettrolitica per la corrosione a piastra piana è un sistema controllato per studiare come un materiale si degrada. Consiste di tre elettrodi primari (di lavoro, controelettrodo e di riferimento), un corpo cella per contenere l'esperimento e una soluzione elettrolitica per simulare un ambiente corrosivo e condurre ioni.
Il sistema è progettato non solo per osservare la corrosione, ma per misurarla con precisione. Ogni componente serve a uno scopo elettrico distinto: il materiale in esame (elettrodo di lavoro), una linea di base di tensione stabile per una misurazione accurata (elettrodo di riferimento) e un percorso per il flusso di corrente senza interferire con la misurazione (controelettrodo).

Il sistema a tre elettrodi: il cuore della cella
L'efficacia di questa configurazione dipende dalla chiara separazione dei ruoli tra i tre elettrodi. Ciò consente di ottenere dati puliti e accurati sul comportamento alla corrosione del materiale.
L'elettrodo di lavoro (il soggetto)
L'elettrodo di lavoro è il campione a piastra piana del materiale che si sta studiando. È il fulcro dell'intero esperimento.
Tutte le misurazioni vengono effettuate su questo componente per determinarne il tasso di corrosione, la resistenza e le proprietà elettrochimiche.
Il controelettrodo (il chiudicircuito)
L'unica funzione del controelettrodo è quella di completare il circuito elettrico. Permette alla corrente di fluire verso o dall'elettrodo di lavoro.
È tipicamente realizzato in un materiale inerte, come il platino, per garantire che non reagisca o interferisca con i processi elettrochimici misurati all'elettrodo di lavoro.
L'elettrodo di riferimento (la linea di base stabile)
L'elettrodo di riferimento è il componente più critico per l'accuratezza della misurazione. Fornisce un potenziale (tensione) costante e stabile che non cambia durante l'esperimento.
Pensatelo come il "livello del mare" per il potenziale elettrico. Tutte le misurazioni del potenziale dell'elettrodo di lavoro vengono effettuate rispetto a questa linea di base inalterabile, garantendo che i dati siano affidabili e ripetibili. Un esempio comune è l'elettrodo argento/cloruro d'argento (Ag/AgCl).
L'ambiente: corpo cella ed elettrolita
Gli elettrodi sono alloggiati all'interno di un ambiente fisico e chimico attentamente controllato che consente alla reazione di corrosione di procedere in modo misurabile.
Il corpo cella (il contenitore inerte)
Il corpo cella è il recipiente fisico, solitamente in vetro o altro materiale chimicamente stabile, che contiene gli elettrodi e la soluzione elettrolitica.
Il suo compito principale è quello di contenere l'esperimento senza reagire con l'elettrolita o influenzare in altro modo i risultati.
L'elettrolita (il mezzo di reazione)
L'elettrolita è la soluzione conduttrice di ioni che circonda gli elettrodi. È progettato per simulare l'ambiente corrosivo specifico che si desidera studiare (ad esempio, acqua di mare, soluzione acida).
Questa soluzione è essenziale in quanto consente agli ioni di migrare tra gli elettrodi, completando il circuito elettrochimico e facilitando il processo di corrosione sulla superficie dell'elettrodo di lavoro.
Comprendere i compromessi e le limitazioni
Sebbene potente, la cella elettrolitica è un modello di laboratorio. Comprendere i suoi limiti è fondamentale per interpretare correttamente i risultati.
Simulazione vs. Realtà
L'ambiente controllato della cella fornisce dati eccellenti ma potrebbe non replicare perfettamente le condizioni del mondo reale, che spesso implicano fluttuazioni di temperatura, sollecitazioni meccaniche o fattori biologici come i biofilm.
L'importanza del posizionamento degli elettrodi
La geometria della configurazione è importante. La distanza e l'orientamento tra gli elettrodi di lavoro, controelettrodo e di riferimento possono influenzare significativamente il campo elettrico e, di conseguenza, l'accuratezza delle misurazioni.
La purezza è fondamentale
I contaminanti nella soluzione elettrolitica possono introdurre reazioni secondarie indesiderate, portando a dati errati e conclusioni scorrette sulla resistenza alla corrosione del materiale.
Applicare questo al tuo obiettivo di ricerca
Il tuo focus sperimentale determinerà quale aspetto dei dati del sistema è più importante per te.
- Se il tuo obiettivo principale è la selezione dei materiali: confronterai la corrente di corrosione misurata da diversi elettrodi di lavoro per classificare quale materiale si comporta meglio in uno specifico elettrolita.
- Se il tuo obiettivo principale è la valutazione dei rivestimenti: il sistema misura l'efficacia con cui un rivestimento sull'elettrodo di lavoro impedisce all'elettrolita di causare corrosione, spesso segnalata da una corrente molto bassa.
- Se il tuo obiettivo principale è la ricerca fondamentale: puoi cambiare sistematicamente una variabile, come la composizione dell'elettrolita, per vedere come influisce sui dati elettrochimici dall'elettrodo di lavoro.
Isolando ogni funzione elettrica, il sistema a tre elettrodi ti consente di tradurre il complesso processo di corrosione in dati precisi e utilizzabili.
Tabella riassuntiva:
| Componente | Funzione primaria | Caratteristica chiave |
|---|---|---|
| Elettrodo di lavoro | Il materiale in esame; il fulcro dell'esperimento. | Il campione a piastra piana studiato per la corrosione. |
| Controelettrodo | Completa il circuito elettrico per consentire il flusso di corrente. | Realizzato in materiale inerte (es. platino) per evitare interferenze. |
| Elettrodo di riferimento | Fornisce una linea di base di tensione stabile per una misurazione accurata. | Essenziale per dati affidabili (es. elettrodo Ag/AgCl). |
| Corpo cella | Un contenitore inerte che contiene l'elettrolita e gli elettrodi. | Chimicamente stabile (es. vetro) per non influenzare i risultati. |
| Elettrolita | La soluzione conduttrice di ioni che simula l'ambiente corrosivo. | Facilita la reazione di corrosione sull'elettrodo di lavoro. |
Pronto a ottenere dati di corrosione precisi e affidabili per la tua ricerca?
La cella elettrolitica a piastra piana è uno strumento potente, ma la sua accuratezza dipende da componenti di alta qualità e da una configurazione esperta. KINTEK è specializzata nella fornitura delle attrezzature e dei materiali di consumo da laboratorio necessari per test elettrochimici superiori.
Sia che tu stia selezionando nuovi materiali, valutando rivestimenti protettivi o conducendo ricerche fondamentali sulla corrosione, abbiamo le soluzioni per supportare il tuo lavoro.
Discutiamo la tua applicazione specifica. Contatta i nostri esperti oggi stesso per assicurarti che il tuo laboratorio sia attrezzato per il successo.
Guida Visiva
Prodotti correlati
- Cella Elettrochimica per Corrosione Piatta
- Cella Elettrolitica in PTFE Cella Elettrochimica Resistente alla Corrosione Sigillata e Non Sigillata
- Cella Elettrochimica Elettrolitica per la Valutazione dei Rivestimenti
- Celle Elettrolitiche PEM Personalizzabili per Diverse Applicazioni di Ricerca
- Cella Elettrolitica Elettrochimica a Cinque Porte
Domande frequenti
- Perché è necessario un sistema di controllo della temperatura costante per i test di corrosione elettrochimica in SBF? Chiave per l'accuratezza di laboratorio
- Quali sono le precauzioni critiche di sicurezza e operative per l'utilizzo di una cella elettrolitica a piastra piana per la corrosione? Garantire test elettrochimici sicuri e accurati
- Quali sono i vantaggi progettuali dell'utilizzo di una cella elettrochimica piatta? Migliorare la precisione dei test di corrosione
- Quali sono le applicazioni comuni di una cella elettrolitica per la corrosione a piastra piatta? Accelerare i test sui materiali e la ricerca
- Quali sono i vantaggi di una cella elettrochimica piana per la corrosione? Ottenere un'analisi precisa di vaiolatura e interstizi

















