L'illusione della manopola
C'è una tentazione nel lavoro di laboratorio di considerare il controllo come un semplice atto meccanico. Si gira una manopola, l'ago si muove e la macchina obbedisce.
In elettrochimica, questa visione è pericolosa.
Una cella elettrolitica non è semplicemente una macchina; è un ambiente caotico in cui si tenta di costringere la natura a muoversi all'indietro. Si utilizza energia per guidare reazioni non spontanee. Per farlo con successo, non si può semplicemente "accenderla".
Devi agire come un architetto dell'ambiente atomico.
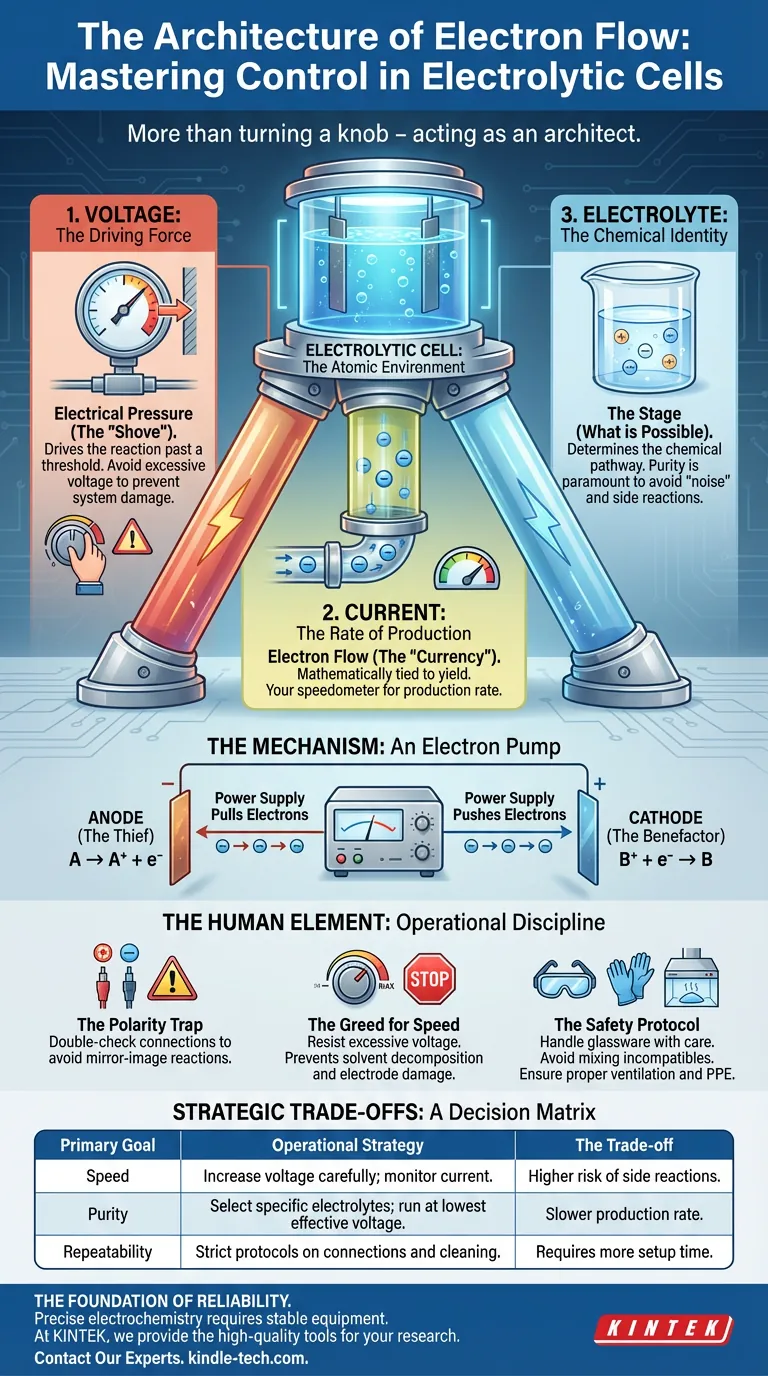
Il controllo in questo contesto è un tripode. Si basa su tre pilastri non negoziabili: Tensione, Corrente e Composizione. Se ne ignori uno, la struttura crolla.
Le tre leve di influenza
Per padroneggiare l'output della tua cella, devi comprendere il ruolo distinto di ciascuna variabile. Sono interconnesse, ma non sono la stessa cosa.
1. Tensione: la forza motrice
Pensa alla tensione come a una pressione elettrica. È la spinta necessaria per far muovere la reazione.
Senza tensione sufficiente, non succede nulla. La barriera alla reazione rimane troppo alta. Tuttavia, più non è sempre meglio. Aumentare la tensione aumenta la velocità, ma solo fino a una soglia. Oltre quel punto, non stai più guidando la reazione, stai danneggiando il sistema.
2. Corrente: la velocità di produzione
La corrente è il flusso di elettroni. Nell'economia della cella elettrolitica, gli elettroni sono la valuta.
La quantità di prodotto che crei è matematicamente legata alla corrente. Se desideri una resa maggiore, devi far passare più carica attraverso il sistema nel tempo. La corrente è il tuo tachimetro.
3. Elettrolita: l'identità chimica
L'elettrolita è il palcoscenico su cui avviene la recita. Determina quale reazione è chimicamente possibile.
Se tensione e corrente sono il motore, l'elettrolita è la destinazione. La purezza qui è fondamentale. Un elettrolita contaminato introduce "rumore" nel sistema, portando a reazioni collaterali che rovinano il prodotto finale.
Il meccanismo: una pompa di elettroni
Per controllare la cella, devi visualizzare cosa sta succedendo agli elettrodi. L'alimentatore esterno agisce come una pompa, creando uno squilibrio che la natura desidera disperatamente correggere.
- All'Anodo (Il Ladro): L'alimentatore strappa gli elettroni. Ciò costringe le specie dell'elettrolita a perdere elettroni (ossidazione).
- Al Catodo (Il Benefattore): L'alimentatore spinge gli elettroni all'interno. Ciò costringe le specie ad acquisire elettroni (riduzione).
Il tuo compito è regolare questa pompa in modo che lo scambio avvenga esattamente come previsto, senza sopraffare la capacità chimica della soluzione.
L'elemento umano: disciplina operativa
La variabile più grande in qualsiasi esperimento è l'operatore. La conoscenza teorica fallisce quando incontra la negligenza pratica.
In chirurgia, una checklist salva vite. In laboratorio, un protocollo salva esperimenti.
La trappola della polarità
Invertire l'anodo e il catodo è un errore semplice con conseguenze profonde. Crea una reazione speculare, producendo le sostanze sbagliate ai poli sbagliati. Controlla i tuoi collegamenti due volte.
L'avidità di velocità
C'è un impulso psicologico a spingere la tensione per finire più velocemente. Resisti.
Una tensione eccessiva porta spesso alla decomposizione del solvente (solitamente acqua) o al degrado della superficie dell'elettrodo. Scambi la purezza con la velocità, e di solito perdi entrambi.
Il protocollo di sicurezza
La chimica è implacabile nei confronti della compiacenza.
- Vetreria: Maneggia la cella con cura. I graffi causati da spazzole metalliche indeboliscono l'integrità strutturale.
- Miscelazioni: Non mescolare mai acidi e basi durante la pulizia. La reazione esotermica risultante può frantumare il recipiente.
- Protezione: Elettroliti corrosivi e gas tossici richiedono un'adeguata ventilazione (cappe chimiche) e DPI.
Compromessi strategici
La perfezione è impossibile. L'ottimizzazione è l'obiettivo. La tua strategia di controllo dovrebbe cambiare in base al tuo obiettivo specifico.
Utilizza questa matrice decisionale per guidare la tua configurazione:
| Obiettivo primario | Strategia operativa | Il compromesso |
|---|---|---|
| Velocità | Aumentare la tensione con cautela; monitorare la corrente. | Maggior rischio di reazioni collaterali. |
| Purezza | Selezionare elettroliti specifici; operare alla tensione efficace più bassa. | Velocità di produzione più lenta. |
| Ripetibilità | Protocolli rigorosi sui collegamenti e sulla pulizia. | Richiede più tempo di configurazione. |
Le fondamenta dell'affidabilità
Non puoi controllare una reazione se non puoi fidarti dei tuoi strumenti.
L'elettrochimica precisa richiede attrezzature che forniscano tensione stabile, corrente costante e materiali durevoli che resistano ad ambienti corrosivi senza contaminare i tuoi risultati.
In KINTEK, comprendiamo la passione dell'ingegnere per la precisione. Siamo specializzati nel fornire attrezzature di laboratorio e consumabili di alta qualità che fungono da partner silenzioso nella tua ricerca. Quando l'hardware è affidabile, sei libero di concentrarti sulla scienza.
Guida Visiva
Prodotti correlati
- Cella Elettrolitica in PTFE Cella Elettrochimica Resistente alla Corrosione Sigillata e Non Sigillata
- Cella Elettrochimica Elettrolitica Super Sigillata
- Cella Elettrolitica Elettrochimica a Cinque Porte
- Cella Elettrolitica Tipo H Tripla Elettrochimica
- Cella Elettrochimica Elettrolitica a Diffusione di Gas Cella di Reazione a Flusso Liquido
Articoli correlati
- Progettazione e standard delle celle elettrolitiche
- Il Partner Silenzioso: Perché la Scelta del Materiale nell'Elettrochimica è una Questione di Fiducia
- La Geometria Silenziosa della Tensione: Rispettare i Limiti dell'Elettrolisi
- Batterie elettrolitiche Una soluzione alla crescente domanda di energia
- L'arte della resistenza: perché la tua cella elettrolitica ha bisogno di spazio per respirare




















