Quando si conduce l'elettrolisi, i fenomeni primari da osservare sono la generazione di bolle di gas sulle superfici degli elettrodi, i cambiamenti nel colore della soluzione e qualsiasi variazione di temperatura. Questi segnali visivi e fisici sono indicatori diretti della reazione elettrochimica sottostante, fornendo un feedback immediato sul fatto che il processo stia procedendo come previsto.
Osservare l'elettrolisi è più che guardare la formazione di bolle. Ogni fenomeno è un dato che rivela l'identità, l'efficienza e la sicurezza della reazione, permettendoti di interpretare ciò che sta accadendo a livello molecolare.

Interpretazione delle osservazioni chiave
Ogni evento osservabile durante l'elettrolisi fornisce un indizio sulle trasformazioni chimiche in atto. Comprendere il significato di questi indizi è essenziale per controllare il risultato.
Evoluzione di gas (bolle) agli elettrodi
Le bolle sono il segno più comune e immediato che una reazione sta avvenendo. Si tratta di prodotti gassosi che si formano direttamente sulle superfici degli elettrodi.
Ad esempio, nell'elettrolisi dell'acqua, vedrai idrogeno gassoso gorgogliare all'elettrodo negativo (catodo) e ossigeno gassoso all'elettrodo positivo (anodo). Il gas specifico prodotto dipende interamente dalla composizione dell'elettrolita.
Cambiamenti nel colore della soluzione
Un cambiamento di colore nell'elettrolita può segnalare diversi eventi. Spesso indica un cambiamento di pH o un cambiamento nella concentrazione di ioni specifici.
Se è presente un indicatore di pH (come la cartina di tornasole o l'indicatore universale), i cambiamenti di colore vicino agli elettrodi rivelano la formazione di ambienti acidi o basici. In alternativa, se l'elettrolita contiene ioni colorati (come gli ioni rame(II) blu), la loro deplezione o formazione può essere tracciata visivamente.
Variazioni di temperatura
L'elettrolisi comporta il passaggio di una corrente elettrica attraverso una soluzione, che genera intrinsecamente del calore a causa della resistenza elettrica (riscaldamento Joule).
Un leggero, graduale aumento della temperatura è normale. Tuttavia, un aumento rapido o eccessivo della temperatura può indicare un'elevata resistenza interna, un processo inefficiente o una reazione collaterale non intenzionale e altamente esotermica.
Cambiamenti degli elettrodi: placcatura o corrosione
Gli elettrodi stessi possono cambiare. In processi come la galvanoplastica, si osserverà uno strato di metallo depositarsi e crescere sul catodo.
Al contrario, se viene utilizzato un anodo reattivo (come rame o zinco), si potrebbe vederlo corrodere o dissolversi visibilmente nella soluzione mentre viene ossidato. Gli elettrodi inerti, come il platino o il carbonio, non dovrebbero mostrare alcun cambiamento.
Comprendere i fattori di controllo
I fenomeni che osservi sono direttamente controllati dai parametri che imposti. Il tipo di elettrodo e di elettrolita determinano cosa può accadere, mentre la tensione e la corrente determinano se accade e quanto velocemente.
Tensione e corrente
La tensione è la forza motrice della reazione; una tensione minima (il potenziale di decomposizione) deve essere applicata affinché l'elettrolisi abbia inizio.
La corrente è una misura della velocità della reazione. È direttamente proporzionale alla velocità con cui gli elettroni vengono trasferiti e, quindi, alla velocità con cui i prodotti vengono formati.
Materiale dell'elettrodo (Inerte vs. Reattivo)
Gli elettrodi inerti (es. platino, grafite) servono solo come superficie per la reazione senza partecipare chimicamente.
Gli elettrodi reattivi (es. rame, zinco, nichel) possono essere ossidati all'anodo, entrando nella soluzione come ioni. Questo è un principio fondamentale nell'elettroaffinazione e nell'elettrodeposizione.
Composizione dell'elettrolita
Gli ioni disponibili nell'elettrolita determinano i potenziali prodotti. In una soluzione con più tipi di ioni, quello più facile da ridurre reagirà al catodo, e quello più facile da ossidare reagirà all'anodo.
Errori comuni e situazioni anomale
L'osservazione del processo ti permette di identificare quando le cose non funzionano correttamente. Queste "situazioni anomale" sono strumenti diagnostici critici.
Nessuna reazione o corrente molto bassa
Ciò indica tipicamente un problema con l'impostazione. La causa potrebbe essere una tensione insufficiente, una connessione elettrica scadente o un elettrolita con resistenza molto elevata.
Colore o precipitato inaspettato
Se osservi un colore non previsto dalla reazione principale o vedi un solido (precipitato) formarsi nella soluzione, ciò suggerisce fortemente la presenza di impurità. Questo indica che sta avvenendo una reazione collaterale non intenzionale.
Generazione eccessiva di calore
Come accennato, un calore significativo indica un'elevata inefficienza. Significa che una gran parte dell'energia elettrica viene sprecata come calore invece di essere utilizzata per guidare il cambiamento chimico desiderato. Questo può anche comportare un rischio per la sicurezza.
Fare la scelta giusta per il tuo obiettivo
La tua interpretazione di queste osservazioni dipende dall'obiettivo del tuo esperimento.
- Se il tuo obiettivo principale è dimostrare un principio di base (es. elettrolisi dell'acqua): Cerca i classici segni di gorgogliamento di gas a entrambi gli elettrodi e usa un indicatore di pH per vedere la formazione di base al catodo e acido all'anodo.
- Se il tuo obiettivo principale è l'elettrodeposizione: L'osservazione più importante è la deposizione uniforme del metallo sul catodo, con corrente e tempo come parametri chiave di controllo.
- Se il tuo obiettivo principale è l'analisi quantitativa (es. verifica delle Leggi di Faraday): Devi assicurare una corrente costante e stabile, poiché questa mette in relazione diretta la quantità di prodotto formato con la carica totale passata attraverso la cella.
Osservando attentamente questi fenomeni, passi da spettatore passivo a controllore attivo del processo elettrochimico.
Tabella riassuntiva:
| Fenomeno | Cosa indica | Approfondimento chiave |
|---|---|---|
| Bolle di gas | Reazione in corso; formazione di prodotto (es. H₂ al catodo, O₂ all'anodo nell'acqua) | Identifica i prodotti gassosi della reazione |
| Cambiamento di colore | Variazione di pH o cambiamento di concentrazione ionica (es. con indicatori o ioni colorati come Cu²⁺) | Rivela l'ambiente chimico e il progresso della reazione |
| Aumento di temperatura | Riscaldamento Joule; calore eccessivo può indicare inefficienza o reazioni collaterali | Monitora la sicurezza del processo e l'efficienza energetica |
| Placcatura/Corrosione dell'elettrodo | Deposizione di metallo (catodo) o dissoluzione (anodo) in processi come l'elettrodeposizione | Critico per applicazioni che richiedono modifiche superficiali |
Ottimizza i tuoi processi di elettrolisi con KINTEK
Stai cercando di ottenere un controllo preciso sui tuoi esperimenti di elettrolisi o applicazioni industriali? Comprendere questi fenomeni osservabili è solo il primo passo. KINTEK è specializzata in attrezzature da laboratorio e materiali di consumo di alta qualità, inclusi elettrodi affidabili, alimentatori stabili e celle di elettrolisi durevoli progettate per prestazioni costanti e risultati accurati.
Che tu stia conducendo ricerche, sviluppando nuovi materiali o aumentando la produzione, i nostri prodotti ti aiutano a monitorare e controllare efficacemente i parametri chiave. Contattaci oggi per discutere come le nostre soluzioni possono migliorare i tuoi flussi di lavoro elettrochimici, migliorare l'efficienza e garantire la sicurezza.
Mettiti in contatto con i nostri esperti ora per trovare l'attrezzatura perfetta per le tue esigenze di laboratorio!
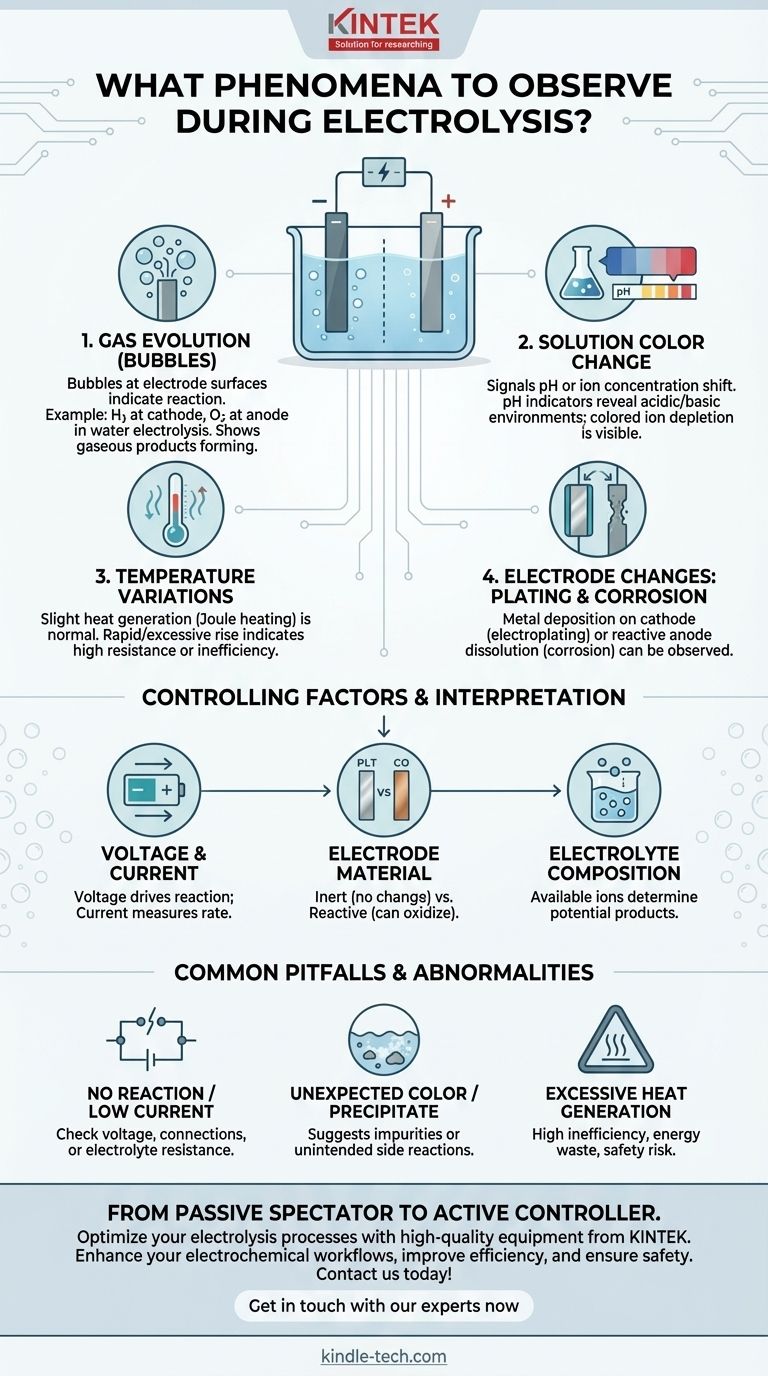
Guida Visiva
Prodotti correlati
- Cella Elettrolitica Tipo H Tripla Elettrochimica
- Cella Elettrochimica Elettrolitica a Diffusione di Gas Cella di Reazione a Flusso Liquido
- Cella Elettrolitica Elettrochimica a Cinque Porte
- Cella Elettrochimica Elettrolitica Super Sigillata
- Cella Elettrolitica in PTFE Cella Elettrochimica Resistente alla Corrosione Sigillata e Non Sigillata
Domande frequenti
- Come devono essere gestiti i guasti o i malfunzionamenti della cella elettrolitica di tipo H? Guida esperta alla risoluzione dei problemi e alla riparazione
- Quali caratteristiche ottiche presenta la cella elettrolitica di tipo H? Finestrini di quarzo di precisione per la fotoelettrochimica
- Quali sono le linee guida chiave per l'uso sicuro della cella elettrolitica di tipo H? Migliori pratiche per il tuo laboratorio
- Qual è l'intervallo di volume tipico per una singola camera della cella elettrolitica di tipo H? Trova la tua capacità di laboratorio ideale
- Cos'è una cella di tipo H? Una guida alle celle elettrochimiche divise per esperimenti accurati



















