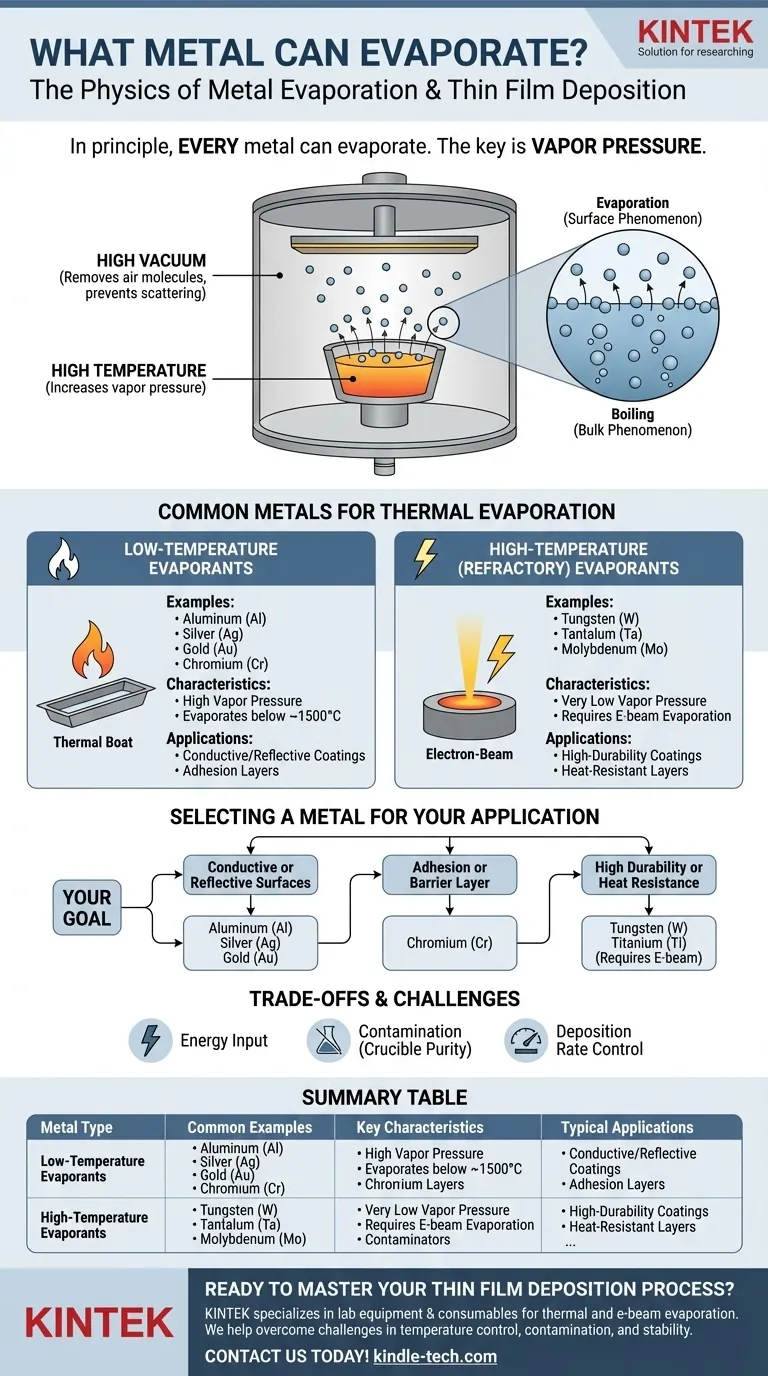
In linea di principio, ogni metallo può evaporare. L'evaporazione è un processo fisico che si verifica quando un elemento o un composto passa dalla fase liquida o solida a quella gassosa. Per i metalli, questo processo è governato dalla temperatura e dalla pressione, con esempi comuni nelle applicazioni tecniche che includono l'evaporazione termica di oro (Au), cromo (Cr) e germanio (Ge) per creare film sottili.
La questione fondamentale non è *se* un metallo possa evaporare, ma *con quanta facilità* lo faccia. Ciò è determinato dalla pressione di vapore intrinseca del metallo, una misura della sua tendenza a diventare gas a una data temperatura. I metalli con una pressione di vapore più elevata sono molto più facili da evaporare.

La fisica dell'evaporazione dei metalli
Per capire quali metalli sono pratici per l'evaporazione, devi prima comprendere i principi che controllano il processo. È un equilibrio tra le proprietà del materiale e l'ambiente che crei.
Cos'è la pressione di vapore?
La pressione di vapore è la pressione esercitata da un vapore in equilibrio con la sua fase solida o liquida. Ogni materiale ha una pressione di vapore, che aumenta significativamente con la temperatura.
Un metallo con un'alta pressione di vapore evaporerà a un ritmo molto più elevato a una data temperatura rispetto a un metallo con una bassa pressione di vapore. Questa è la proprietà più importante che ne determina l'idoneità all'evaporazione.
Il ruolo della temperatura e del vuoto
Per ottenere un tasso di evaporazione utile per la maggior parte dei metalli, sono necessarie temperature molto elevate, spesso centinaia o migliaia di gradi Celsius.
Questo processo viene quasi sempre eseguito in una camera ad alto vuoto. Il vuoto rimuove le molecole d'aria che altrimenti colliderebbero con gli atomi metallici in evaporazione, disperdendoli e impedendo loro di raggiungere il substrato bersaglio.
Evaporazione vs. Ebollizione
L'evaporazione è un fenomeno superficiale in cui i singoli atomi acquisiscono energia sufficiente per sfuggire. L'ebollizione è un fenomeno di massa in cui la pressione di vapore eguaglia la pressione atmosferica circostante, formando bolle all'interno del materiale.
Nella deposizione sotto vuoto, l'obiettivo è ottenere un tasso di evaporazione controllato, non far bollire violentemente il materiale sorgente.
Metalli comuni utilizzati nell'evaporazione termica
I metalli sono spesso classificati in base alle temperature richieste per evaporarli efficacemente sotto vuoto.
Evaporanti a bassa temperatura
Questi metalli hanno pressioni di vapore relativamente elevate, il che consente loro di essere evaporati a temperature gestibili (tipicamente inferiori a 1500°C). Sono ampiamente utilizzati per creare rivestimenti.
Esempi comuni includono Alluminio (Al), Argento (Ag), Oro (Au) e Cromo (Cr). La loro facilità d'uso li rende elementi fondamentali nell'elettronica e nell'ottica.
Evaporanti ad alta temperatura (refrattari)
I metalli refrattari hanno pressioni di vapore estremamente basse e punti di fusione molto elevati, il che li rende difficili da evaporare con semplici metodi termici.
Metalli come Tungsteno (W), Tantalo (Ta) e Molibdeno (Mo) richiedono tecniche specializzate, come l'evaporazione a fascio di elettroni, che può raggiungere le temperature localizzate molto più elevate necessarie.
Comprendere i compromessi
Scegliere semplicemente un metallo non è sufficiente; devi comprendere le sfide pratiche e i limiti del processo di evaporazione.
La sfida dei metalli refrattari
Evaporare un metallo come il tungsteno richiede un enorme apporto energetico. L'attrezzatura è più complessa e costosa, poiché deve essere in grado di generare e resistere a temperature estreme senza contaminare il processo.
Purezza della sorgente e contaminazione
Anche il materiale del crogiolo o della "barchetta" che contiene il metallo può essere una fonte di contaminazione. Ad alte temperature, il materiale del crogiolo stesso può evaporare o reagire con il metallo fuso, introducendo impurità nel film sottile finale.
Tasso di deposizione e controllo
Il tasso di evaporazione di un metallo può cambiare drasticamente con piccole fluttuazioni di temperatura. Mantenere un processo di deposizione stabile e ripetibile richiede un controllo della temperatura altamente preciso, il che è più facile per i materiali a bassa temperatura rispetto ai metalli refrattari.
Selezione di un metallo per la tua applicazione
La scelta del metallo dovrebbe essere guidata interamente dall'obiettivo del film sottile che stai creando.
- Se la tua attenzione principale è creare superfici conduttive o riflettenti: Metalli come Alluminio (Al), Argento (Ag) e Oro (Au) sono scelte eccellenti grazie alla loro elevata conducibilità/riflettività e alla relativa facilità di evaporazione.
- Se la tua attenzione principale è uno strato di adesione o di barriera: Il Cromo (Cr) è una scelta standard poiché aderisce bene a molti substrati come il vetro, rendendolo un ottimo strato intermedio per deposizioni successive.
- Se la tua attenzione principale richiede elevata durabilità o resistenza al calore: Dovrai utilizzare un metallo refrattario come Tungsteno (W) o Titanio (Ti), ma preparati per un processo di evaporazione a fascio di elettroni più complesso e ad alta intensità energetica.
In definitiva, comprendere la pressione di vapore di un metallo è la chiave per padroneggiare la sua evaporazione per qualsiasi applicazione tecnica.
Tabella riassuntiva:
| Tipo di metallo | Esempi comuni | Caratteristiche principali | Applicazioni tipiche |
|---|---|---|---|
| Evaporanti a bassa temperatura | Alluminio (Al), Oro (Au), Argento (Ag), Cromo (Cr) | Alta pressione di vapore, evapora sotto ~1500°C | Rivestimenti conduttivi, superfici riflettenti, strati di adesione |
| Evaporanti ad alta temperatura (refrattari) | Tungsteno (W), Tantalo (Ta), Molibdeno (Mo) | Pressione di vapore molto bassa, richiede evaporazione a fascio di elettroni | Rivestimenti ad alta durabilità, strati resistenti al calore |
Pronto a padroneggiare il tuo processo di deposizione di film sottili?
Scegliere il metallo e la tecnica di evaporazione corretti è fondamentale per ottenere risultati coerenti e di alta qualità. KINTEK è specializzata in apparecchiature da laboratorio e materiali di consumo per l'evaporazione termica e a fascio di elettroni, fornendo gli strumenti precisi e il supporto esperto di cui hai bisogno.
Aiutiamo i nostri clienti nella ricerca e sviluppo e nella produzione a superare sfide come il controllo della temperatura, la contaminazione e la stabilità del tasso di deposizione. Contattaci oggi per discutere la tua applicazione specifica e lascia che i nostri esperti ti guidino verso la soluzione ottimale per le esigenze del tuo laboratorio.
Contattaci tramite il nostro Modulo di Contatto
Guida Visiva