L'Illusione della Semplicità
In laboratorio, i momenti più critici sono spesso i più silenziosi.
Tendiamo a ossessionarci sulla chimica complessa: i reagenti esotici, la tensione precisa, la resa teorica. Ma in elettrochimica, l'intero esperimento dipende da un atto meccanico che richiede meno di cinque minuti: l'installazione degli elettrodi.
Sembra banale. Metti il metallo nel vetro. Accendi l'alimentazione.
Ma questa visione è pericolosa.
Una cella elettrolitica non è solo un contenitore; è un circuito. L'elettrodo è l'interfaccia dove il mondo fisico incontra il mondo chimico. Se quell'interfaccia è difettosa, anche solo di un millimetro, i dati non sono solo leggermente errati. Sono finzione.
Ecco come affrontare il processo di installazione con la precisione di un ingegnere e la disciplina di un chirurgo.
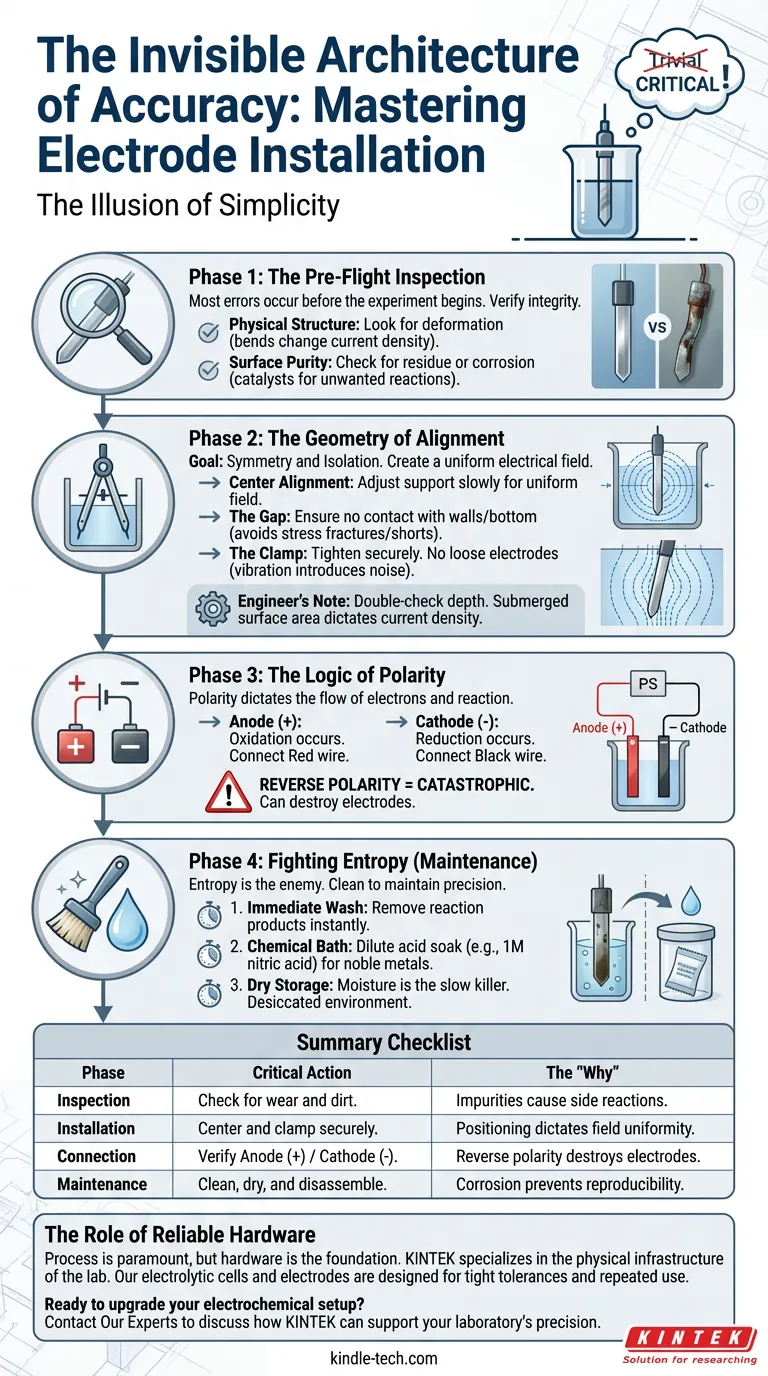
Fase 1: L'Ispezione Pre-Volo
La maggior parte degli errori si verifica prima che l'esperimento inizi.
Spesso presumiamo che, poiché un elettrodo appare solido, sia funzionale. Questo è un bias cognitivo noto come "ciò che vedi è tutto ciò che c'è". Tuttavia, in elettrochimica, la chimica superficiale è tutto.
Prima che l'elettrodo tocchi la cella, devi verificarne l'integrità:
- Struttura Fisica: Cerca deformazioni. Un elettrodo piegato altera la distribuzione della densità di corrente.
- Purezza della Superficie: Controlla residui o corrosione. Un granello di polvere non è solo polvere; è un catalizzatore per reazioni collaterali indesiderate.
Se la superficie è compromessa, l'esperimento è condannato prima ancora di iniziare. Le superfici pulite non sono un lusso; sono un prerequisito.
Fase 2: La Geometria dell'Allineamento
Una volta completata l'ispezione, passiamo all'installazione fisica.
Questo è un gioco di geometria. L'obiettivo è simmetria e isolamento.
Quando abbassi gli elettrodi nella cella, stai cercando di creare un campo elettrico uniforme. Se un elettrodo è inclinato, il campo si deforma. Le velocità di reazione cambiano. La riproducibilità svanisce.
Le Regole di Posizionamento
- Allineamento Centrale: Regola lentamente il meccanismo di supporto. L'elettrodo dovrebbe essere l'asse attorno al quale ruota la cella.
- Lo Spazio: Assicurati che l'elettrodo non tocchi mai il fondo o le pareti della cella. Il contatto con il vetro può causare fratture da stress. Il contatto con l'altro elettrodo provoca un cortocircuito.
- Il Morsetto: Una volta posizionato, stringi i morsetti di supporto. Non fare affidamento sulla gravità o sull'attrito. Un elettrodo allentato vibra, e la vibrazione introduce rumore nei tuoi dati.
Nota dell'Ingegnere: Ricontrolla la profondità. L'area superficiale sommersa determina la densità di corrente. Se la profondità cambia, i tuoi calcoli sono errati.
Fase 3: La Logica della Polarità
La chimica ha una direzione.
Collegare l'alimentatore non è come collegare un tostapane. La polarità detta il flusso degli elettroni e, quindi, il flusso della reazione.
- Anodo (+): Qui avviene l'ossidazione.
- Catodo (-): Qui avviene la riduzione.
Un'inversione qui è catastrofica. Non solo ferma l'esperimento; spesso distrugge gli elettrodi forzando l'ossidazione su un materiale progettato per la riduzione.
Traccia sempre il filo dalla sorgente alla cella. Rosso all'Anodo. Nero al Catodo. Non fidarti della tua memoria. Fidati del filo.
Fase 4: Combattere l'Entropia (Manutenzione)
L'esperimento non finisce quando viene tolta l'alimentazione.
L'entropia è il nemico delle attrezzature di laboratorio. Se lasci un elettrodo bagnato di elettrolita, la corrosione inizia immediatamente. I sali cristallizzano. Il metallo si degrada.
Per mantenere il "fascino" dei macchinari precisi, devi pulirli.
- Lavaggio Immediato: Rimuovi immediatamente i prodotti di reazione.
- Bagno Chimico: Per i metalli nobili come il platino, un ammollo in acido diluito (es. acido nitrico 1M) ripristina la superficie.
- Conservazione Asciutta: L'umidità è il killer lento. Conserva i componenti in un ambiente disidratato.
Se stai conservando la cella a lungo termine, smontala. Lasciare l'elettrolita in una cella sigillata significa invitare il degrado.
Checklist Riassuntiva
Un professionista tratta questo processo come un sistema, non come un compito.
| Fase | Azione Critica | Il "Perché" |
|---|---|---|
| Ispezione | Controllare usura e sporco. | Le impurità causano reazioni collaterali. |
| Installazione | Centrare e fissare saldamente. | Il posizionamento determina l'uniformità del campo. |
| Connessione | Verificare Anodo (+) / Catodo (-). | L'inversione di polarità distrugge gli elettrodi. |
| Manutenzione | Pulire, asciugare e smontare. | La corrosione impedisce la riproducibilità. |
Il Ruolo di Hardware Affidabile
Il processo è fondamentale, ma l'hardware è la base.
Non puoi eseguire un lavoro preciso con morsetti instabili o metalli impuri. Il miglior protocollo del mondo non può compensare un elettrodo che si degrada in modo imprevedibile o una cella che si deforma sotto stress termico.
È qui che interviene KINTEK.
Siamo specializzati nell'infrastruttura fisica del laboratorio. Le nostre celle elettrolitiche e i nostri elettrodi in platino o grafite sono progettati per resistere ai rigori dell'uso ripetuto. Costruiamo le nostre attrezzature con tolleranze precise che gli ingegneri apprezzano, garantendo che quando centri un elettrodo, questo rimanga centrato.
La tua ricerca merita attrezzature altrettanto disciplinate quanto te.
Pronto ad aggiornare il tuo setup elettrochimico?
Contatta i Nostri Esperti per discutere come KINTEK può supportare la precisione del tuo laboratorio.
Guida Visiva
Prodotti correlati
- Elettrodi di Riferimento Calomel Argento Cloruro Solfato di Mercurio per Uso di Laboratorio
- Elettrodo Elettrochimico a Disco Metallico
- Elettrodo a disco rotante (anello-disco) RRDE / compatibile con PINE, ALS giapponese, Metrohm svizzero al carbonio vetroso platino
- Elettrodo a disco rotante in platino per applicazioni elettrochimiche
- Elettrodo a lastra di platino per applicazioni di laboratorio su batterie
Articoli correlati
- Elettrodi di pseudo-riferimento Quando e come usarli
- Elettrodi di riferimento comuni negli studi elettrochimici
- Fondamenti di elettrochimica:Condizioni e precauzioni per l'uso di diversi elettrodi di riferimento
- Uso e cura degli elettrodi di riferimento
- Progettazione e applicazione di elettrodi di riferimento nelle batterie al litio




















