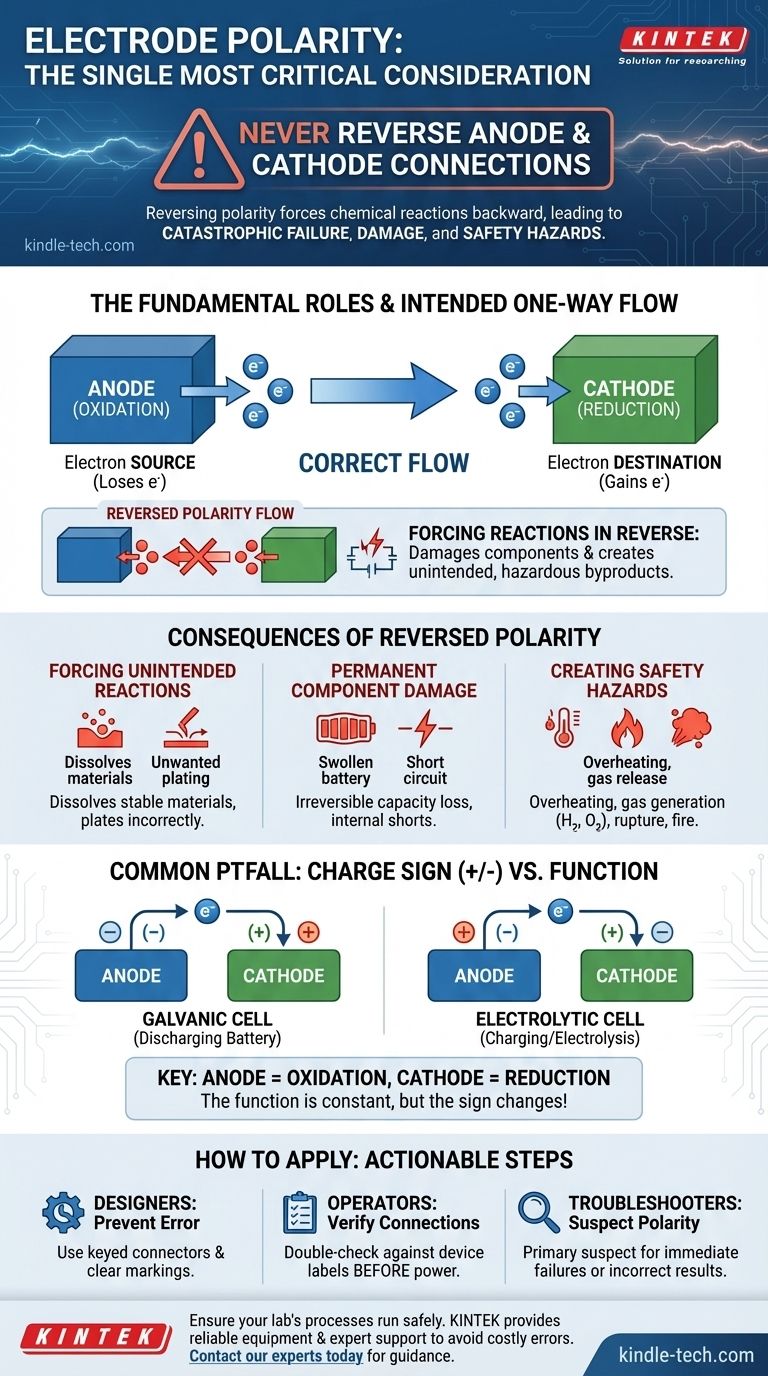
La considerazione singola più critica per la polarità degli elettrodi è che i collegamenti tra anodo e catodo non devono mai essere invertiti. Questa non è una mera convenzione; invertire la polarità può forzare le reazioni chimiche a funzionare al contrario, portando a danni immediati e spesso irreversibili ai componenti, a un funzionamento errato del sistema o persino a significativi pericoli per la sicurezza.
La polarità degli elettrodi detta la direzione fondamentale della reazione chimica prevista. Invertirla è come forzare un motore a funzionare in retromarcia: agisce attivamente contro la progettazione del sistema, portando a un guasto catastrofico anziché al risultato desiderato.

I Ruoli Fondamentali di Anodo e Catodo
Per comprendere perché l'inversione della polarità sia così dannosa, dobbiamo prima stabilire i ruoli specifici e non intercambiabili dei due elettrodi.
L'Anodo: Sede dell'Ossidazione
L'anodo è definito come l'elettrodo in cui avviene l'ossidazione. Questo è il processo in cui una specie chimica perde elettroni.
Considera l'anodo come la "sorgente" nel circuito elettrico, che rilascia elettroni nel sistema a seguito della reazione chimica.
Il Catodo: Sede della Riduzione
Il catodo è l'elettrodo in cui avviene la riduzione. Questo è il processo complementare in cui una specie chimica acquisisce gli elettroni rilasciati dall'anodo.
Il catodo funge da "destinazione", consumando elettroni per completare la reazione chimica e il circuito elettrico.
Perché Questa Direzione è Importante
L'intero sistema elettrochimico — che si tratti di una batteria, un sensore o un bagno di elettrodeposizione — è progettato attorno a questo flusso specifico e unidirezionale di elettroni dall'anodo al catodo. I materiali per ciascun elettrodo sono scelti precisamente per la loro capacità di eseguire l'ossidazione o la riduzione in modo efficiente.
Le Conseguenze dell'Inversione della Polarità
Collegare anodo e catodo in modo errato forza la corrente a fluire nella direzione sbagliata, obbligando ciascun elettrodo a svolgere una funzione chimica per la quale non è stato progettato.
Forzare Reazioni Non Intenzionali
Quando la polarità viene invertita, si applica una tensione che tenta di far ossidare il catodo e ridurre l'anodo. Ciò può dissolvere materiali che dovrebbero essere stabili o depositare materiali su superfici dove non dovrebbero trovarsi, creando sottoprodotti chimici indesiderati.
Danni Permanenti ai Componenti
In una batteria ricaricabile, ad esempio, invertire la connessione durante la carica può causare la deposizione di litio metallico sull'anodo, riducendo permanentemente la capacità della batteria e creando un rischio di cortocircuito interno. Nell'elettrodeposizione, inizierebbe a dissolvere proprio l'oggetto che si intende rivestire.
Creazione di Pericoli per la Sicurezza
Forzare reazioni sbagliate può portare a esiti pericolosi. Il surriscaldamento è comune e nei sistemi acquosi, la decomposizione dell'acqua può generare rapidamente gas idrogeno e ossigeno infiammabili. Nelle applicazioni ad alta potenza come i sistemi a batteria, ciò può portare a rigonfiamento, rottura o incendio.
Errori Comuni da Evitare
La definizione di anodo e catodo è costante, ma il loro segno di carica (+ o -) può essere fonte di confusione perché dipende dal tipo di cella elettrochimica.
Celle Galvaniche vs. Elettrolitiche
In una cella galvanica (quella che produce energia, come una batteria in scarica), l'anodo è il terminale negativo. La reazione di ossidazione spontanea spinge fuori gli elettroni.
In una cella elettrolitica (quella che consuma energia, come una batteria in carica o per l'elettrolisi), l'anodo è il terminale positivo. Una fonte di alimentazione esterna estrae elettroni da esso per guidare una reazione non spontanea.
È fondamentale riconoscere che, sebbene il segno possa cambiare, la funzione non cambia: l'anodo è sempre dove avviene l'ossidazione.
L'Importanza di un'Etichettatura Chiara
A causa di questa potenziale confusione, è necessario fare affidamento sulle etichette (+/-) e sulla documentazione del sistema. I progettisti hanno tenuto conto del tipo di cella. Non dare mai per scontato che l'anodo sia sempre negativo o positivo senza conoscerne il contesto.
Come Applicare Questo al Tuo Progetto
Il tuo approccio alla polarità dipende dal tuo ruolo nel ciclo di vita del sistema.
- Se il tuo obiettivo principale è la progettazione di un sistema: Il tuo obiettivo è prevenire errori dell'utente. Utilizza connettori a chiave che possono essere inseriti solo in un modo e fornisci marcature chiare e permanenti per i terminali
+e-. - Se il tuo obiettivo principale è l'utilizzo di apparecchiature: Il tuo obiettivo è la verifica. Controlla sempre i collegamenti rispetto alle marcature del dispositivo o agli schemi prima di applicare l'alimentazione, rendendolo un passaggio critico in qualsiasi lista di controllo.
- Se il tuo obiettivo principale è la diagnosi di un guasto: Il tuo obiettivo è la diagnosi. La polarità invertita dovrebbe essere un sospetto primario se un componente si guasta immediatamente dopo la connessione o se un processo produce risultati inaspettati e errati.
Rispettare correttamente la polarità degli elettrodi è il fondamento per qualsiasi sistema elettrochimico sicuro, efficiente e funzionale.
Tabella Riassuntiva:
| Aspetto | Polarità Corretta | Polarità Invertita |
|---|---|---|
| Funzione Anodo | Ossidazione (perde elettroni) | Forzato ad eseguire la riduzione |
| Funzione Catodo | Riduzione (acquisisce elettroni) | Forzato ad eseguire l'ossidazione |
| Risultato del Sistema | Funzionamento progettato ed efficiente | Guasto catastrofico, danni |
| Rischio per la Sicurezza | Basso (se utilizzato correttamente) | Alto (surriscaldamento, generazione di gas, incendio) |
Assicurati che i processi elettrochimici del tuo laboratorio funzionino in modo sicuro ed efficiente. Una polarità errata degli elettrodi può portare a danni immediati alle apparecchiature, pericoli per la sicurezza e esperimenti rovinati. KINTEK è specializzata nel fornire apparecchiature e materiali di consumo di laboratorio affidabili, supportati da un supporto tecnico esperto per aiutarti a evitare errori costosi. Non mettere a rischio la tua ricerca o la tua sicurezza: contatta oggi i nostri esperti per ricevere indicazioni sulla selezione e l'utilizzo dei sistemi elettrochimici giusti per le esigenze del tuo laboratorio.
Guida Visiva
Prodotti correlati
- Elettrodi di Riferimento Calomel Argento Cloruro Solfato di Mercurio per Uso di Laboratorio
- Elettrodo Elettrochimico a Disco Metallico
- Elettrodo a disco rotante (anello-disco) RRDE / compatibile con PINE, ALS giapponese, Metrohm svizzero al carbonio vetroso platino
- Elettrodo a disco rotante in platino per applicazioni elettrochimiche
- Elettrodo a lastra di platino per applicazioni di laboratorio su batterie
Domande frequenti
- Qual è l'elettrodo di riferimento nella potenziometria? La chiave per misurazioni stabili e accurate
- Qual è la funzione di un elettrodo di riferimento? Padroneggia la precisione nella ricostruzione di reattori a tre elettrodi
- Quale tipo di elettrodo può essere utilizzato come punto di riferimento? Seleziona quello giusto per misurazioni accurate
- Perché la scelta di un elettrodo di riferimento di alta qualità è fondamentale nella sintesi elettrochimica? | KINTEK
- Qual è lo scopo dell'elettrodo di riferimento? Ottenere misurazioni elettrochimiche stabili e accurate



















