Nella sua essenza, il principio dell'elettrodeposizione è il processo di utilizzo di una corrente elettrica continua per ridurre gli ioni metallici disciolti da una soluzione e formare un sottile rivestimento metallico solido su un oggetto conduttivo. Questa reazione elettrochimica controllata consente di "placcare" un metallo su un altro, alterando fondamentalmente le proprietà superficiali del materiale di base.
L'intero processo dipende dalla creazione di un circuito elettrolitico. In questo circuito, l'elettricità guida una reazione chimica non spontanea, costringendo gli ioni metallici a carica positiva in un bagno liquido ad accettare elettroni e a depositarsi come strato metallico neutro sulla superficie bersaglio.
I componenti fondamentali di un sistema di elettrodeposizione
Per comprendere il principio in pratica, è necessario prima comprendere i suoi quattro componenti essenziali che lavorano insieme all'interno di una cella elettrolitica.
L'elettrolita (il bagno)
L'elettrolita è una soluzione contenente un'alta concentrazione di ioni metallici che si desidera depositare. Questo è tipicamente preparato sciogliendo sali metallici (come solfato di rame o cloruro di nichel) in acqua. Il bagno contiene anche altri additivi per controllare la qualità del rivestimento finale.
Il catodo (il substrato)
Il catodo è l'oggetto che si intende rivestire. È collegato al terminale negativo dell'alimentatore. Questa carica negativa attira gli ioni metallici a carica positiva dall'elettrolita.
L'anodo (la fonte di metallo)
L'anodo è collegato al terminale positivo dell'alimentatore. Può essere di due tipi:
- Anodo attivo: Realizzato con lo stesso metallo che viene placcato. Si dissolve lentamente, reintegrando gli ioni metallici nell'elettrolita man mano che vengono depositati sul catodo.
- Anodo inerte: Realizzato con un materiale non reattivo (come platino o carbonio). Non si dissolve ma serve a completare il circuito elettrico. In questo caso, gli ioni metallici nel bagno si esauriscono nel tempo.
L'alimentatore
Un alimentatore a corrente continua (CC) funge da motore per l'intero processo. Fornisce il potenziale elettrico necessario per guidare gli elettroni verso il catodo e attirarli dall'anodo, forzando l'avvenimento della reazione di deposizione.
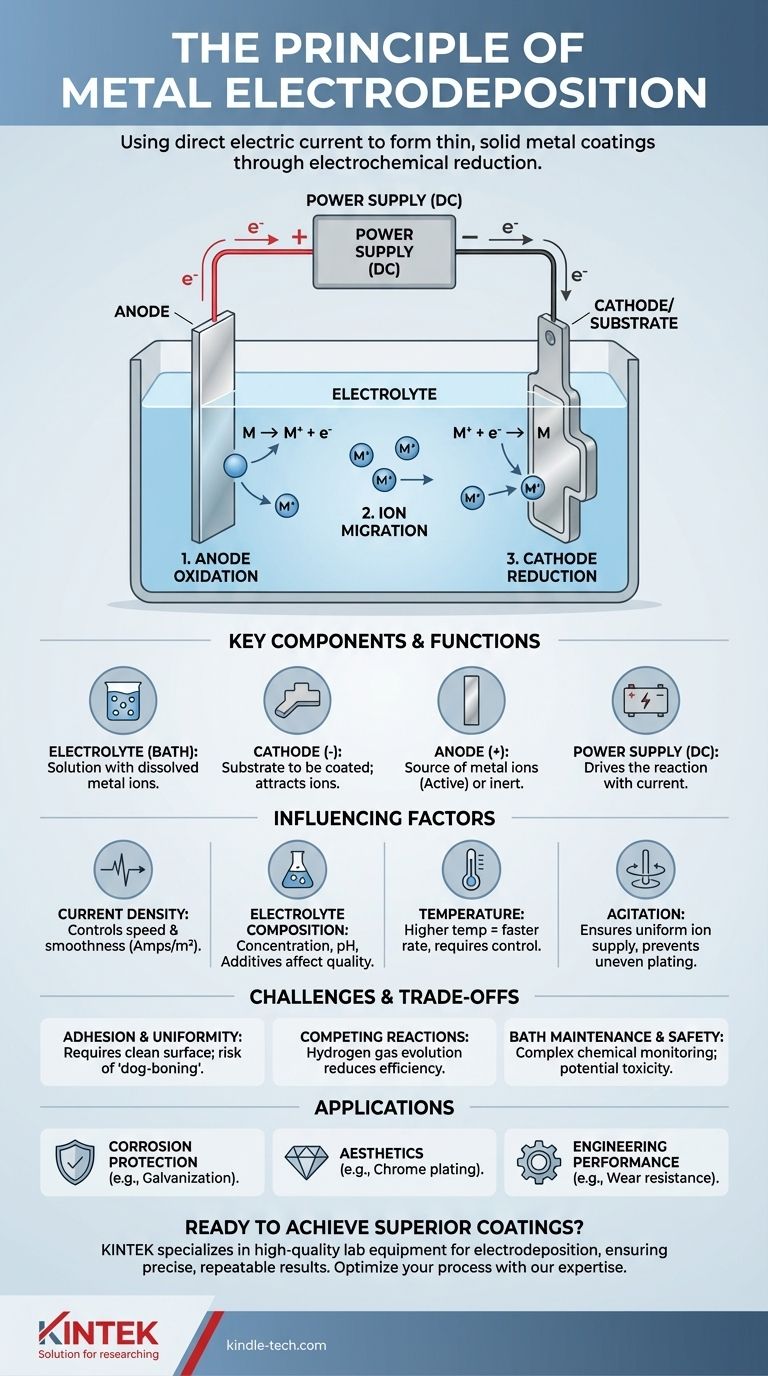
Il processo elettrochimico, passo dopo passo
Il processo di deposizione è un ciclo continuo di ossidazione e riduzione guidato dall'alimentatore esterno.
Passaggio 1: Ossidazione all'anodo
All'anodo positivo si verifica una reazione di ossidazione. Se l'anodo è attivo, i suoi atomi metallici perdono elettroni e diventano ioni a carica positiva, dissolvendosi nell'elettrolita. Ciò mantiene costante la fornitura di ioni metallici.
Passaggio 2: Migrazione degli ioni nell'elettrolita
Gli ioni metallici a carica positiva (cationi) presenti nell'elettrolita vengono attratti attraverso la soluzione verso il catodo a carica negativa. Contemporaneamente, gli ioni negativi (anioni) migrano verso l'anodo positivo, mantenendo la soluzione elettricamente neutra.
Passaggio 3: Riduzione al catodo
Questo è il passaggio di deposizione. Quando gli ioni metallici raggiungono il catodo, acquisiscono elettroni forniti dall'alimentatore. Questa reazione di riduzione neutralizza la loro carica, facendoli precipitare dalla soluzione e legarsi alla superficie come atomi metallici solidi, costruendo il rivestimento strato dopo strato.
Fattori chiave che influenzano la qualità della deposizione
La qualità, lo spessore e l'aspetto del rivestimento finale non sono automatici. Dipendono dal controllo attento di diverse variabili chiave.
Densità di corrente
Questa è la quantità di corrente per unità di superficie del catodo (misurata in Ampere/m²).
- Una bassa densità di corrente si traduce in un rivestimento lento ma spesso più liscio e uniforme.
- Una alta densità di corrente accelera la deposizione ma può portare a depositi ruvidi, porosi o bruciati se non gestita correttamente.
Composizione dell'elettrolita
La concentrazione degli ioni metallici, il livello di pH e la presenza di additivi (come brillantanti e livellanti) hanno un impatto enorme. Questi additivi possono alterare la struttura cristallina del metallo che si deposita, modificandone la finitura da opaca a a specchio.
Temperatura
Temperature più elevate del bagno generalmente aumentano la conducibilità dell'elettrolita e la velocità di deposizione. Tuttavia, temperature eccessivamente elevate possono causare reazioni secondarie indesiderate o la decomposizione degli additivi.
Agitazione
Mescolare o agitare in altro modo il bagno è fondamentale. Assicura che una fornitura fresca di ioni metallici raggiunga la superficie del catodo, prevenendo l'esaurimento localizzato che causa una placcatura non uniforme, specialmente su forme complesse.
Comprendere i compromessi e le sfide
Sebbene potente, l'elettrodeposizione è un processo preciso con punti di fallimento comuni.
Adesione e uniformità del rivestimento
Il fattore più critico per il successo è la preparazione del substrato. Una superficie sporca o ossidata comporterà una scarsa adesione, causando il distacco o la sfaldatura del rivestimento. Inoltre, la corrente elettrica si concentra naturalmente su bordi e angoli acuti, portando a depositi più spessi lì e depositi più sottili nelle rientranze, un problema noto come effetto "dog-boning" (a forma di osso di cane).
Reazioni competitive
La principale reazione competitiva, specialmente negli elettroliti acquosi, è la riduzione dell'acqua per produrre gas idrogeno al catodo. Questo processo consuma corrente elettrica che altrimenti verrebbe utilizzata per la deposizione del metallo, riducendo l'efficienza complessiva. In alcuni casi, l'idrogeno assorbito può anche rendere fragile il substrato.
Manutenzione del bagno e sicurezza
I bagni di elettrodeposizione sono sistemi chimici complessi che richiedono un monitoraggio e una regolazione costanti di pH, temperatura e concentrazioni chimiche. Molte soluzioni di placcatura industriali, come quelle contenenti cianuro o cromo esavalente, sono altamente tossiche e pongono rischi significativi per l'ambiente e la sicurezza degli operatori.
Scegliere l'opzione giusta per la tua applicazione
Comprendere il principio fondamentale ti permette di adattare il processo al tuo obiettivo specifico.
- Se il tuo obiettivo principale è la protezione dalla corrosione: Il tuo obiettivo è uno strato denso e non poroso, spesso utilizzando un metallo sacrificale come lo zinco sull'acciaio (zincatura) o un metallo nobile come l'oro.
- Se il tuo obiettivo principale è l'estetica: Devi controllare attentamente la densità di corrente e utilizzare additivi specifici come i brillantanti per ottenere una superficie liscia e riflettente, come si vede nella placcatura al cromo o al nichel.
- Se il tuo obiettivo principale sono le prestazioni ingegneristiche (ad esempio, resistenza all'usura): Hai bisogno di un controllo preciso dello spessore e della durezza, spesso ottenuto con cromo duro o rivestimenti in nichel chimico, dove una forte adesione è fondamentale.
Controllando il flusso di ioni ed elettroni, puoi trasformare la superficie di un materiale per soddisfare un'esigenza ingegneristica o estetica specifica.

Tabella riassuntiva:
| Componente chiave | Ruolo nell'elettrodeposizione |
|---|---|
| Elettrolita (Bagno) | Soluzione contenente ioni metallici disciolti da depositare. |
| Catodo (Substrato) | L'oggetto da rivestire; attrae ioni metallici positivi. |
| Anodo (Fonte di metallo) | Fonte di ioni metallici (attivo) o elettrodo inerte. |
| Alimentatore (CC) | Fornisce la corrente per guidare la reazione non spontanea. |
| Densità di corrente | Controlla la velocità di deposizione e la qualità del rivestimento (uniformità). |
| Additivi del bagno | Influenzano le proprietà finali del rivestimento (es. brillantezza, durezza). |
Pronto a ottenere rivestimenti metallici superiori nel tuo laboratorio?
Comprendere i principi dell'elettrodeposizione è il primo passo. Implementarla efficacemente richiede le attrezzature e i materiali di consumo giusti. KINTEK è specializzata in attrezzature da laboratorio di alta qualità per l'elettrodeposizione e altri processi di ingegneria delle superfici, aiutandoti a ottenere risultati precisi, affidabili e ripetibili.
Sia che tu ti concentri sulla ricerca, sul controllo qualità o sullo sviluppo di nuovi rivestimenti, la nostra esperienza può supportare le esigenze del tuo laboratorio.
Contatta oggi i nostri esperti per discutere come possiamo aiutarti a ottimizzare il tuo processo di elettrodeposizione!
Guida Visiva
Prodotti correlati
- Elettrodo Elettrochimico a Disco Metallico
- Crogiolo in rame privo di ossigeno per rivestimento a evaporazione a fascio elettronico e barchetta di evaporazione
- Lamiera di schiuma di rame e nichel
- Lamiere di metallo di alta purezza in oro, platino e rame
- Elettrodo a foglio d'oro per elettrochimica Elettrodo d'oro
Domande frequenti
- Quali sono i metodi raccomandati per la protezione superficiale di diversi tipi di elettrodi a disco metallici? Guida essenziale per la longevità
- Quali materiali possono essere utilizzati per gli elettrodi a disco metallico? Scegliere il metallo giusto per il tuo esperimento elettrochimico
- Qual è la funzione principale degli elettrodi metallici nell'elettrocoagulazione? Ottimizza la tua strategia di bonifica delle microplastiche
- Quale ispezione iniziale dovrebbe essere eseguita su un elettrodo a disco metallico prima dell'uso? Garantire risultati elettrochimici accurati
- Qual è la durata prevista di un elettrodo a disco metallico? Prolungane la vita con la cura adeguata



















