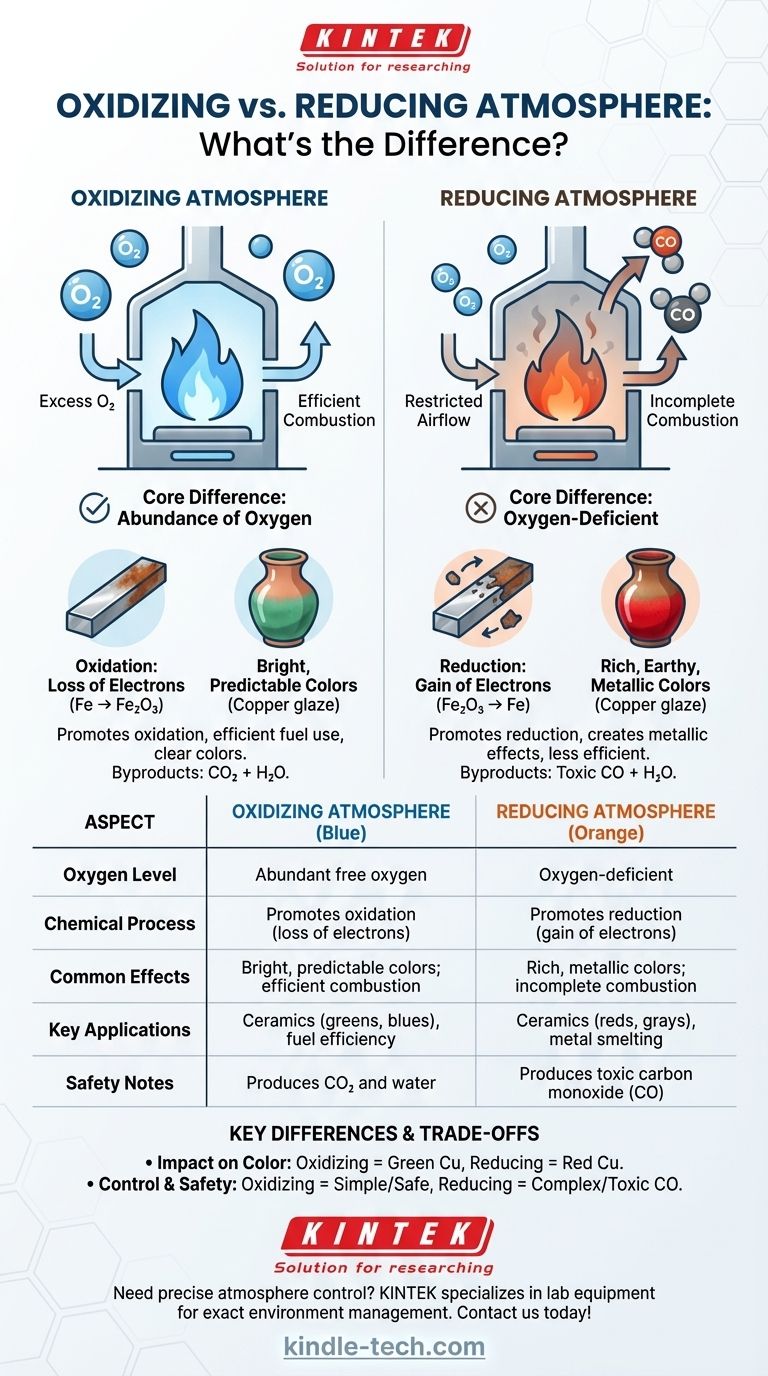
In sostanza, la differenza tra un'atmosfera ossidante e una riducente è la disponibilità di ossigeno. Un'atmosfera ossidante ha un'abbondanza di ossigeno libero, che promuove reazioni chimiche come la combustione e la corrosione. Un'atmosfera riducente è carente di ossigeno e strappa attivamente atomi di ossigeno dai materiali, invertendo il processo di ossidazione.
La scelta tra un'atmosfera ossidante o riducente è un meccanismo di controllo fondamentale nella scienza dei materiali e nella chimica. Non si tratta solo dell'ambiente; è uno strumento utilizzato per modificare deliberatamente lo stato chimico e le proprietà fisiche di un materiale.
Cos'è un'atmosfera ossidante?
Un'atmosfera ossidante è lo stato "predefinito" in cui viviamo, definito dalla presenza di ossigeno in eccesso. Nelle applicazioni ad alta temperatura come forni o fornaci, viene mantenuta garantendo un'offerta costante e abbondante di aria fresca.
Il ruolo dell'ossigeno in eccesso
La caratteristica chiave è che c'è più ossigeno disponibile di quanto sia necessario per bruciare completamente qualsiasi combustibile presente. Questo ossigeno in eccesso è chimicamente attivo e pronto a reagire con altri materiali.
Il processo chimico: Ossidazione
L'ossidazione è una reazione chimica in cui una sostanza perde elettroni. Sebbene altri elementi possano causare ciò, in questo contesto, quasi sempre comporta che una sostanza si leghi con l'ossigeno. Questo è lo stesso processo fondamentale che causa la ruggine del ferro o la combustione pulita di un fuoco.
Effetti e applicazioni comuni
In un fuoco ossidante, il combustibile brucia in modo efficiente e completo, producendo il massimo calore con poca o nessuna fuliggine. Nella ceramica, produce colori chiari, brillanti e spesso prevedibili da smalti e corpi argillosi (ad esempio, il ferro produce marroni e rossi, il rame produce verdi e blu).
Cos'è un'atmosfera riducente?
Un'atmosfera riducente è un ambiente privo di ossigeno. Viene deliberatamente creata in un forno o in una fornace limitando l'ingresso di aria o introducendo più combustibile di quanto l'aria disponibile possa bruciare.
Il ruolo del combustibile incombusto
Con ossigeno insufficiente per una combustione completa, il combustibile incombusto rilascia composti come il monossido di carbonio (CO) e l'idrogeno. Questi composti sono chimicamente instabili e cercano aggressivamente atomi di ossigeno per legarsi.
Il processo chimico: Riduzione
La riduzione è l'opposto dell'ossidazione; è una reazione chimica in cui una sostanza acquista elettroni. In questo ambiente, il monossido di carbonio "ruba" attivamente atomi di ossigeno dagli ossidi metallici all'interno dell'argilla o degli smalti, riducendoli a uno stato più metallico.
Effetti e applicazioni comuni
Un fuoco riducente è spesso più freddo e più fumoso, segno di combustione incompleta. È essenziale per processi come la fusione del metallo dal minerale. Nella ceramica, crea colori terrosi e metallici ricchi, complessi e spesso imprevedibili (ad esempio, il ferro produce blu e grigi profondi, il rame produce rossi vibranti).
Comprendere le differenze chiave e i compromessi
La decisione di utilizzare un'atmosfera rispetto all'altra è interamente guidata dal risultato desiderato, ma comporta significativi compromessi.
Impatto sul colore e sulle proprietà del materiale
Questa è la differenza più visibile. Uno smalto contenente ossido di rame diventerà verde in un'atmosfera ossidante. Lo stesso smalto, se cotto in un'atmosfera riducente, vedrà il suo ossigeno rimosso, riducendo il rame alla sua forma metallica e creando un rosso brillante.
Controllo ed efficienza
Ottenere un'atmosfera ossidante è semplice: fornire molta aria. Creare un'atmosfera riducente richiede una gestione attiva, come la chiusura di una serranda per privare il fuoco di ossigeno. Ciò rende il processo meno efficiente in termini di carburante, poiché non si estrae tutta l'energia potenziale dal combustibile.
Sicurezza e sottoprodotti
I fuochi ossidanti producono principalmente anidride carbonica (CO₂) e acqua. I fuochi riducenti, a causa della combustione incompleta, producono quantità significative di monossido di carbonio (CO), un gas incolore, inodore e altamente tossico. Una ventilazione adeguata è assolutamente fondamentale quando si crea un'atmosfera riducente.
Come scegliere l'atmosfera giusta
La tua scelta dipende interamente dal tuo materiale e dal tuo obiettivo. L'atmosfera non è una condizione di fondo; è un ingrediente attivo nel processo chimico.
- Se il tuo obiettivo principale sono colori brillanti, stabili e l'efficienza del carburante: Usa un'atmosfera ossidante garantendo un flusso d'aria costante e abbondante al tuo forno o fornace.
- Se il tuo obiettivo principale sono effetti ricchi, terrosi o metallici nella ceramica: Usa un'atmosfera riducente limitando attentamente il flusso d'aria a temperature specifiche per forzare la riduzione chimica degli ossidi metallici.
- Se il tuo obiettivo principale è la fusione di minerali o la prevenzione della formazione di scaglie superficiali sull'acciaio: Usa un'atmosfera fortemente riducente per rimuovere l'ossigeno dal minerale o impedirne la formazione sulla superficie del metallo.
Padroneggiare l'interazione tra ossigeno e calore ti dà un controllo preciso sulla forma e sulla funzione finale del tuo materiale.

Tabella riassuntiva:
| Aspetto | Atmosfera Ossidante | Atmosfera Riducente |
|---|---|---|
| Livello di Ossigeno | Ossigeno libero abbondante | Carente di ossigeno |
| Processo Chimico | Promuove l'ossidazione (perdita di elettroni) | Promuove la riduzione (guadagno di elettroni) |
| Effetti Comuni | Colori brillanti, prevedibili; combustione efficiente | Colori ricchi, metallici; combustione incompleta |
| Applicazioni Chiave | Ceramica (verdi, blu), efficienza del carburante | Ceramica (rossi, grigi), fusione di metalli |
| Note di Sicurezza | Produce CO₂ e acqua | Produce monossido di carbonio (CO) tossico |
Hai bisogno di un controllo preciso dell'atmosfera per i processi del tuo laboratorio? KINTEK è specializzata in attrezzature e materiali di consumo da laboratorio, offrendo forni e fornaci che forniscono un controllo esatto su ambienti ossidanti o riducenti. Che tu stia sviluppando nuovi materiali, testando ceramiche o conducendo esperimenti ad alta temperatura, le nostre soluzioni garantiscono risultati accurati e ripetibili. Contattaci oggi per discutere come possiamo migliorare le capacità del tuo laboratorio!
Guida Visiva