In termini tecnici, una cella elettrolitica è un tipo specifico di cella elettrochimica. Sebbene rientri in questa ampia categoria, è fondamentale capire che "cella elettrochimica" descrive anche un altro dispositivo—la cella galvanica—che svolge la funzione esattamente opposta.
La distinzione cruciale è questa: una cella elettrolitica utilizza energia elettrica esterna per forzare una reazione chimica che non avverrebbe spontaneamente. Consuma energia. Al contrario, una cella galvanica (come una batteria) utilizza una reazione chimica spontanea per produrre energia elettrica.

La Funzione Principale: Forzare una Reazione Chimica
Cos'è l'Elettrolisi?
L'elettrolisi è il processo che utilizza una corrente elettrica continua (DC) per innescare una reazione chimica non spontanea. In termini semplici, si tratta di usare l'elettricità per far avvenire un cambiamento chimico.
Il dispositivo in cui avviene questo processo è la cella elettrolitica.
Il Ruolo dell'Alimentazione Esterna
La caratteristica distintiva di una cella elettrolitica è la sua necessità di una fonte di alimentazione esterna, come una batteria o un alimentatore. Questa tensione esterna supera la barriera energetica naturale della reazione, costringendo le sostanze chimiche a reagire.
Componenti Chiave
Una cella elettrolitica è composta da due elettrodi, un anodo e un catodo, immersi in una soluzione liquida chiamata elettrolita. La fonte di alimentazione esterna estrae elettroni dall'anodo (ossidazione) e li spinge al catodo (riduzione), innescando il cambiamento chimico desiderato.
Elettrolitica vs. Galvanica: L'ombrello della "Cella Elettrochimica"
Il termine cella elettrochimica è una categoria genitore per qualsiasi dispositivo che converte energia chimica in energia elettrica e viceversa. Comprendere i due tipi principali è essenziale per chiarezza.
Celle Elettrolitiche: Consumatori di Energia
Queste celle consumano energia elettrica per produrre un cambiamento chimico. Il loro scopo principale è creare sostanze o alterare materiali attraverso una reazione forzata.
Un esempio comune è l'uso di una cella elettrolitica per scindere l'acqua (H₂O) in idrogeno e ossigeno gassoso, un processo che richiede un significativo apporto energetico.
Celle Galvaniche (Voltaiche): Produttori di Energia
Queste celle fanno l'opposto. Sfruttano una reazione chimica spontanea per generare una corrente elettrica. Questo è il principio fondamentale alla base di tutte le batterie comuni.
Quando si usa una batteria, si sta usando una cella galvanica per convertire l'energia chimica immagazzinata in energia elettrica utilizzabile.
Perché la Distinzione è Importante
Chiamare una cella elettrolitica "cella elettrochimica" è tecnicamente corretto ma impreciso. È come chiamare un quadrato un "rettangolo". Sebbene vero, omette le proprietà specifiche che lo definiscono. La differenza chiave è sempre la direzione della conversione energetica.
Applicazioni Comuni e Compromessi
Dove viene Utilizzata l'Elettrolisi
La capacità di forzare reazioni chimiche ha un immenso valore industriale. Le celle elettrolitiche sono essenziali per produrre idrogeno puro per il carburante, raffinare metalli come alluminio e rame dai minerali e galvanizzare oggetti con un sottile strato di metallo come cromo o oro.
Il Compromesso Principale: Costo Energetico
La principale limitazione dell'elettrolisi è il suo elevato consumo energetico. Poiché si sta forzando una reazione non spontanea, il processo richiede sempre più energia rispetto all'energia chimica che si immagazzina o al valore del prodotto creato. Questo costo energetico è la considerazione economica e ambientale centrale per qualsiasi processo di elettrolisi industriale.
Come Identificare la Cella Giusta per il Tuo Obiettivo
- Se il tuo obiettivo principale è immagazzinare energia o creare materiali (come carburante a idrogeno o alluminio puro): Hai a che fare con una cella elettrolitica, che consuma elettricità per innescare una reazione chimica.
- Se il tuo obiettivo principale è generare energia da una fonte chimica (come una batteria): Hai a che fare con una cella galvanica (o voltaica), che produce elettricità da una reazione spontanea.
- Se il tuo obiettivo principale è il campo scientifico generale che copre entrambi i processi: Dovresti usare il termine generico cella elettrochimica.
In definitiva, comprendere la direzione del flusso di energia—se viene consumata o prodotta—è la chiave per distinguere tra questi dispositivi fondamentali.
Tabella Riassuntiva:
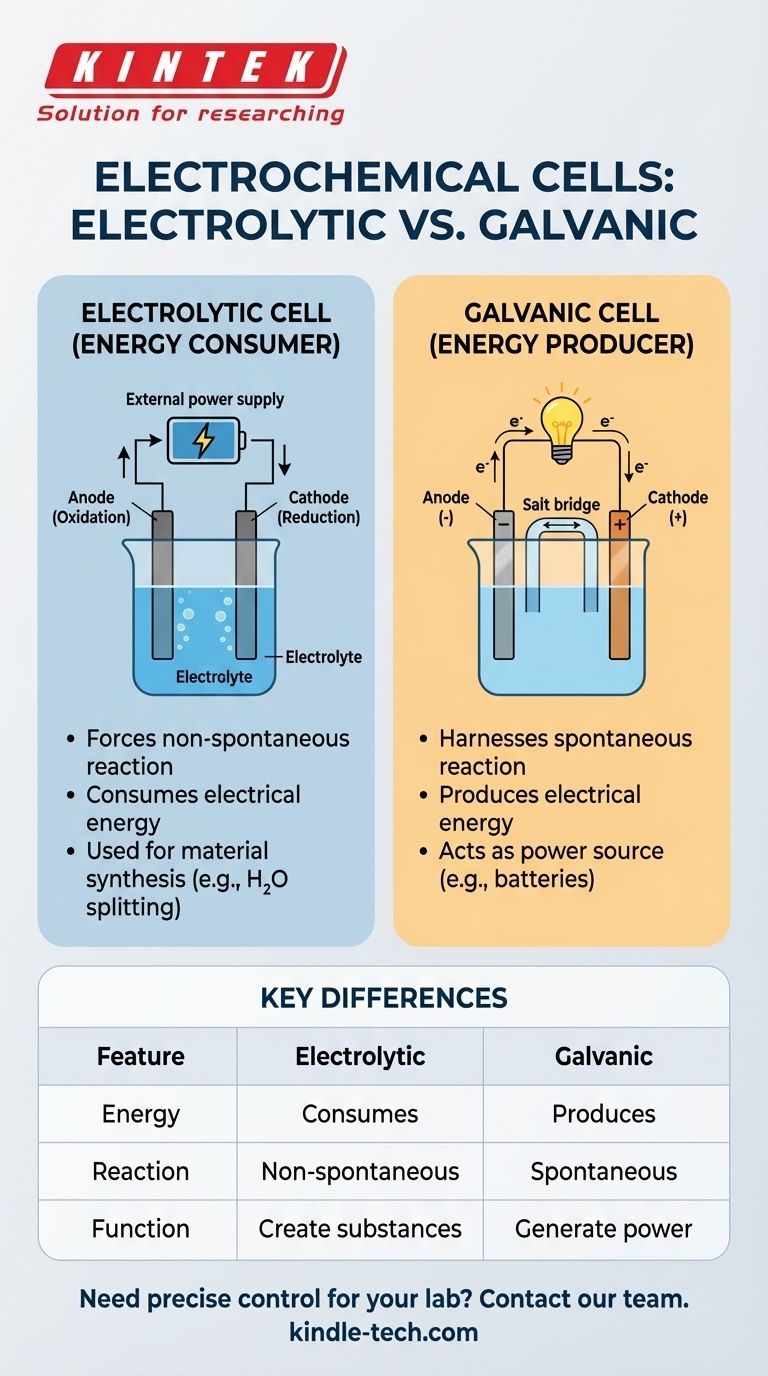
| Caratteristica | Cella Elettrolitica | Cella Galvanica |
|---|---|---|
| Conversione Energetica | Consuma energia elettrica | Produce energia elettrica |
| Tipo di Reazione | Non spontanea (forzata) | Spontanea |
| Funzione Primaria | Creare sostanze (es. H₂, metalli raffinati) | Generare energia (es. batterie) |
| Fonte di Alimentazione | Richiede una fonte esterna (es. batteria, alimentatore) | È la fonte di alimentazione stessa |
Hai bisogno di un controllo preciso sulle reazioni chimiche nel tuo laboratorio?
Che la tua ricerca riguardi la sintesi di materiali, la galvanoplastica o l'accumulo di energia, disporre dell'attrezzatura giusta è fondamentale. KINTEK è specializzata in attrezzature e materiali di consumo da laboratorio di alta qualità, comprese celle elettrochimiche e alimentatori, progettati per affidabilità e precisione.
Lascia che i nostri esperti ti aiutino a selezionare la configurazione perfetta per la tua applicazione specifica. Contatta il nostro team oggi stesso per discutere le tue esigenze di laboratorio e scoprire come KINTEK può supportare i tuoi obiettivi di ricerca.
Guida Visiva
Prodotti correlati
- Celle Elettrolitiche PEM Personalizzabili per Diverse Applicazioni di Ricerca
- Cella Elettrochimica per Elettrolisi Spettrale a Strato Sottile
- Cella Elettrochimica Elettrolitica a Diffusione di Gas Cella di Reazione a Flusso Liquido
- Cella Elettrochimica Elettrolitica al Quarzo per Esperimenti Elettrochimici
- Cella Elettrolitica in PTFE Cella Elettrochimica Resistente alla Corrosione Sigillata e Non Sigillata
Domande frequenti
- Qual è la procedura corretta per spegnere l'esperimento dopo l'elettrolisi? Una guida alla sicurezza passo-passo
- Quali sono le configurazioni di apertura per le versioni non sigillate e sigillate della cella di elettrolisi? Ottimizza la tua configurazione elettrochimica
- Qual è la procedura di conservazione corretta per una cella elettrolitica e i suoi componenti? Una guida passo-passo per preservare l'accuratezza
- Quali sono le precauzioni per riscaldare o sterilizzare una cella elettrolitica? Evitare di danneggiare i componenti sensibili
- Quali sono i rischi di un controllo improprio della tensione in una cella elettrolitica? Evitare danni costosi e inefficienze



















