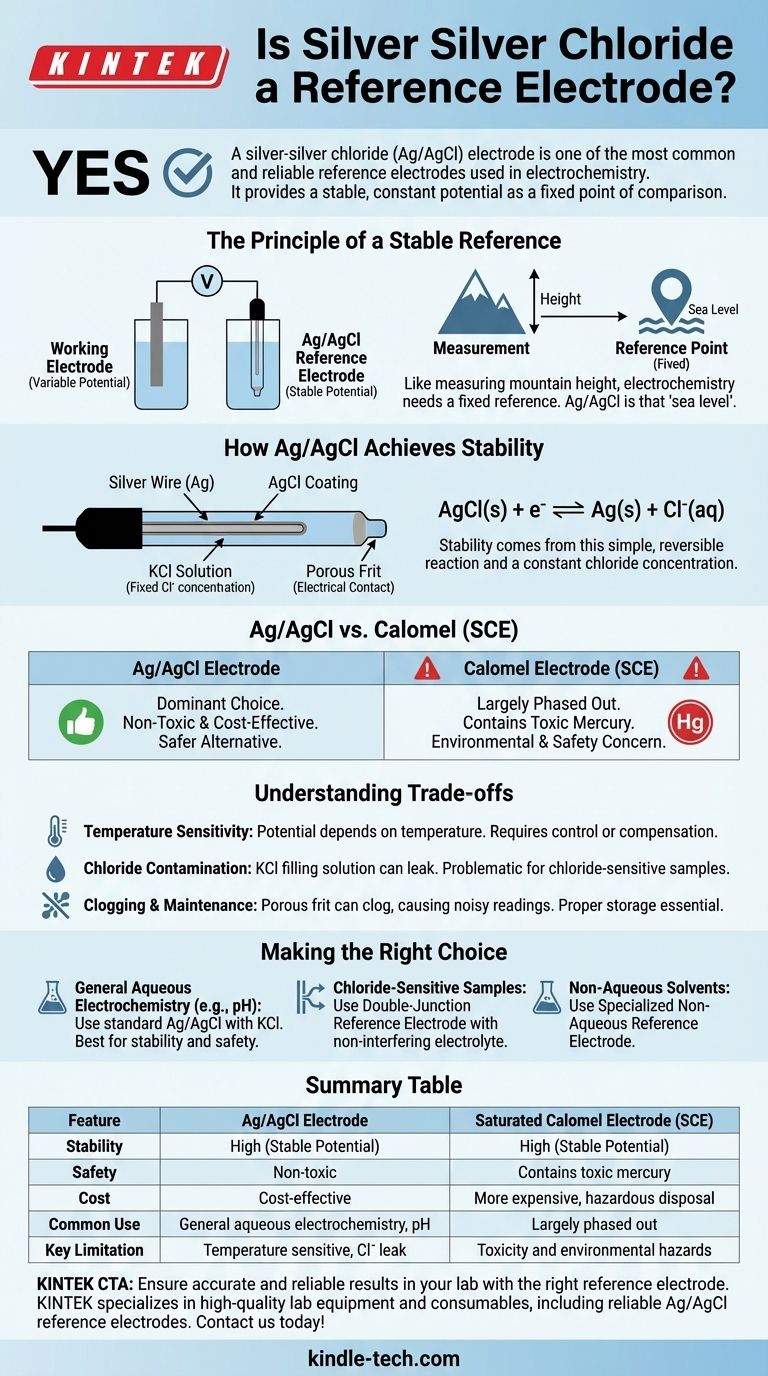
Sì, l'elettrodo argento-cloruro d'argento (Ag/AgCl) è uno degli elettrodi di riferimento più comuni e affidabili utilizzati in elettrochimica. Fornisce un potenziale stabile e costante che funge da punto fisso di riferimento, consentendo di misurare accuratamente il potenziale di un altro elettrodo (l'elettrodo di lavoro) all'interno di una cella elettrochimica. Questa stabilità lo rende indispensabile per applicazioni che vanno dalla misurazione del pH alla voltammetria ciclica.
La funzione principale di un elettrodo di riferimento è fornire una linea di base di tensione immutabile. L'elettrodo Ag/AgCl ottiene ciò attraverso un equilibrio chimico specifico e stabile, rendendolo uno standard fidato ed economico nell'elettrochimica moderna.

Il principio di un riferimento stabile
Per capire perché l'elettrodo Ag/AgCl è così efficace, dobbiamo prima capire cosa rende un buon riferimento. Una misurazione elettrochimica è sempre un confronto di potenziale tra due punti.
Cos'è un elettrodo di riferimento?
Un elettrodo di riferimento è una semicella con un potenziale elettrodico noto e stabile. Il suo compito è rimanere costante, indipendentemente dai cambiamenti che si verificano nell'altra metà della cella (l'elettrodo di lavoro e la soluzione campione).
Pensala come alla misurazione dell'altezza di una montagna. Hai bisogno di un punto di riferimento fisso, come il livello del mare, per ottenere una misurazione significativa. In elettrochimica, l'elettrodo di riferimento è il livello del mare.
Come l'Ag/AgCl ottiene la stabilità
La stabilità dell'elettrodo Ag/AgCl deriva da una reazione chimica semplice e reversibile. È costituito da un filo d'argento rivestito da un sottile strato di cloruro d'argento (AgCl), tutto immerso in una soluzione con una concentrazione fissa di ioni cloruro (Cl⁻), tipicamente cloruro di potassio (KCl).
Il potenziale è stabilito dall'equilibrio tra l'argento metallico solido e il suo sale:
AgCl(s) + e⁻ ⇌ Ag(s) + Cl⁻(aq)
Poiché la concentrazione della soluzione di cloruro all'interno dell'elettrodo viene mantenuta costante, il potenziale di questa semireazione rimane eccezionalmente stabile.
Ag/AgCl rispetto ad altri elettrodi di riferimento
L'elettrodo Ag/AgCl non è l'unica opzione, ma i suoi vantaggi lo hanno reso una scelta dominante rispetto agli standard più vecchi come l'elettrodo a calomelano saturo (SCE).
L'ascesa dell'Ag/AgCl
La ragione principale della diffusione dell'Ag/AgCl è la sua sicurezza e le sue prestazioni. È relativamente economico da produrre e, soprattutto, non tossico.
Il declino dell'elettrodo a calomelano (SCE)
L'elettrodo a calomelano, che utilizza una pasta di mercurio/cloruro mercuroso, era un tempo uno standard comune. Tuttavia, è stato in gran parte eliminato in molti laboratori.
La ragione principale è la tossicità. Il mercurio è un materiale pericoloso, il che rende l'uso, lo stoccaggio e lo smaltimento degli elettrodi a calomelano una significativa preoccupazione ambientale e di sicurezza.
Comprendere i compromessi
Sebbene l'elettrodo Ag/AgCl sia un'ottima scelta per uso generale, non è privo di limitazioni. Comprendere questi compromessi è fondamentale per misurazioni accurate.
Sensibilità alla temperatura
Il potenziale di un elettrodo Ag/AgCl dipende dalla temperatura. Per lavori di altissima precisione, la temperatura della cella deve essere controllata e riportata, oppure deve essere utilizzata una sonda a compensazione di temperatura.
Contaminazione da cloruri
L'elettrodo è riempito con una soluzione concentrata di KCl. Una piccola quantità di questa soluzione può fuoriuscire dal setto poroso all'estremità dell'elettrodo e nel campione. Se il tuo esperimento è sensibile agli ioni cloruro, questa può essere una fonte di errore.
Ostruzione e manutenzione
Il setto poroso che consente il contatto elettrico con il campione può ostruirsi, portando a letture di potenziale rumorose o fluttuanti. Una corretta conservazione (con la punta immersa nella sua soluzione di riempimento) e una manutenzione regolare sono essenziali per una lunga durata e risultati accurati.
Fare la scelta giusta per la tua applicazione
La scelta dell'elettrodo di riferimento e della soluzione di riempimento corretta è fondamentale per il successo dell'esperimento. La tua scelta dipende interamente dalla chimica del tuo campione.
- Se stai eseguendo elettrochimica acquosa generale (come la maggior parte delle misurazioni di pH o ioni): Un elettrodo Ag/AgCl con una soluzione di riempimento standard di KCl è quasi sempre la scelta migliore grazie alla sua stabilità e sicurezza.
- Se il tuo campione reagisce o è sensibile agli ioni cloruro: Devi utilizzare un elettrodo di riferimento a "doppia giunzione", in cui una camera esterna con un elettrolita non interferente (come il nitrato di potassio) isola l'elemento interno Ag/AgCl dal tuo campione.
- Se lavori in solventi non acquosi: Avrai bisogno di un elettrodo di riferimento non acquoso specializzato, poiché gli elettrodi acquosi standard non funzioneranno correttamente e contamineranno il tuo solvente.
In definitiva, la scelta dell'elettrodo di riferimento corretto consiste nell'assicurarsi che rimanga un osservatore inerte e stabile della reazione chimica che si desidera studiare.
Tabella riassuntiva:
| Caratteristica | Elettrodo Ag/AgCl | Elettrodo a calomelano saturo (SCE) |
|---|---|---|
| Stabilità | Alta (potenziale stabile) | Alta (potenziale stabile) |
| Sicurezza | Non tossico | Contiene mercurio tossico |
| Costo | Conveniente | Più costoso, smaltimento pericoloso |
| Uso comune | Elettrochimica acquosa generale, misurazione del pH | In gran parte eliminato a causa di problemi di sicurezza |
| Limitazione chiave | Sensibile alla temperatura, potenziale contaminazione da cloruri | Tossicità e rischi ambientali |
Assicurati risultati accurati e affidabili nel tuo laboratorio con il giusto elettrodo di riferimento. KINTEK è specializzata in attrezzature e materiali di consumo di alta qualità per laboratori, inclusi elettrodi di riferimento Ag/AgCl affidabili, adattati alle tue applicazioni elettrochimiche. I nostri esperti possono aiutarti a selezionare l'elettrodo perfetto per mantenere la stabilità ed evitare la contaminazione nei tuoi esperimenti. Contattaci oggi per migliorare la precisione e la sicurezza del tuo laboratorio!
Guida Visiva
Prodotti correlati
- Elettrodi di Riferimento Calomel Argento Cloruro Solfato di Mercurio per Uso di Laboratorio
- Elettrodo di riferimento al solfato di rame per uso di laboratorio
- Cella Elettrochimica Elettrolitica a Diffusione di Gas Cella di Reazione a Flusso Liquido
- Elettrodo Elettrochimico in Carbonio Vetroso
- Elettrodo Elettrochimico in Grafite, Elettrodo a Disco e Asta in Grafite
Domande frequenti
- In che modo la scelta degli elettrodi di riferimento, come Ag/AgCl o Hg/HgO, è correlata al pH dell'elettrolita nei test di reazione di evoluzione dell'idrogeno (HER)?
- Qual è la manutenzione raccomandata per la soluzione di riempimento di un elettrodo di riferimento? Una Guida per Letture Stabili e Accurate
- Quale elettrodo viene utilizzato come riferimento di massa? Padroneggia la chiave per misurazioni elettrochimiche accurate
- Quale elettrodo viene utilizzato come elettrodo di riferimento per la misurazione dei potenziali di semicella? Comprendere lo standard universale
- Qual è l'elettrodo di riferimento nella potenziometria? La chiave per misurazioni stabili e accurate











