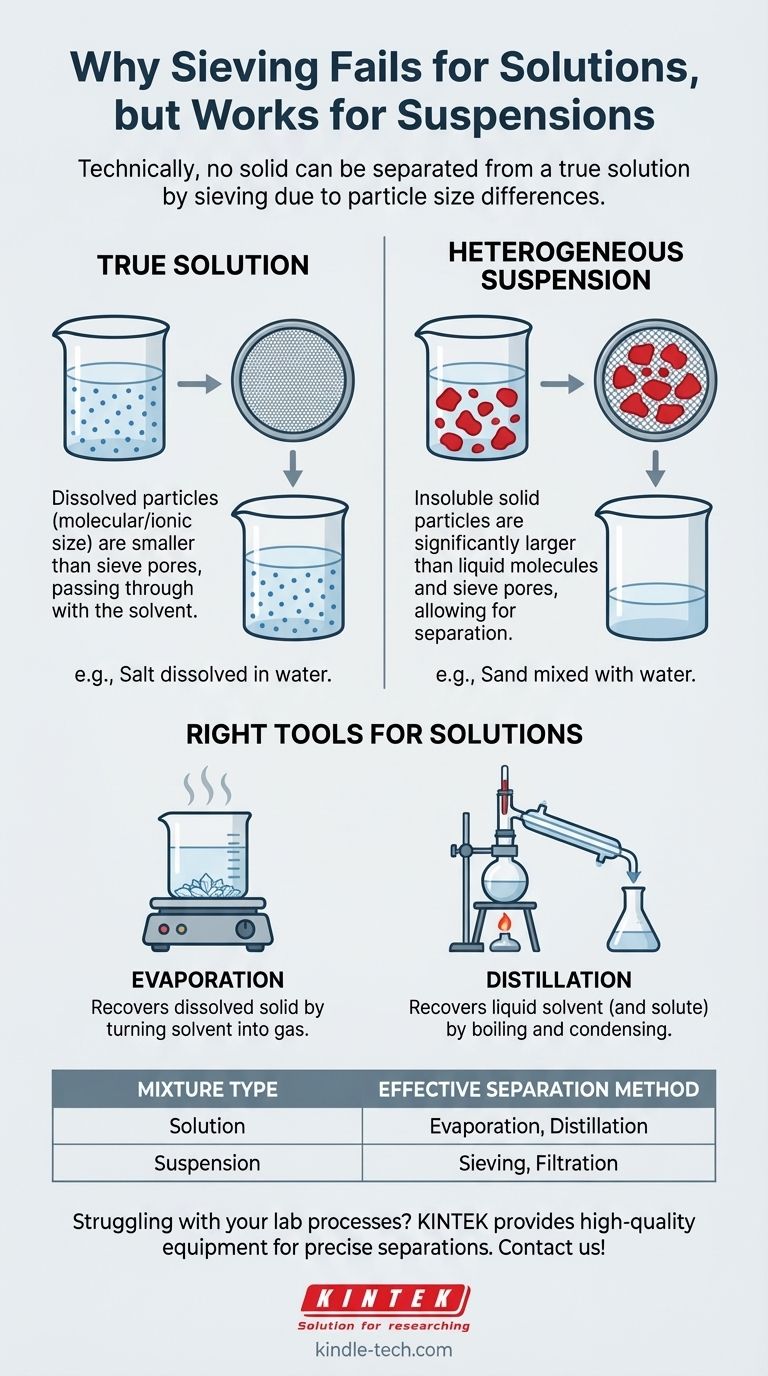
Tecnicamente, nessun solido può essere separato da una vera soluzione per setacciatura. Questo perché, in una soluzione, il solido si è disciolto in singole molecole o ioni, che sono troppo piccoli per essere catturati dai pori di qualsiasi setaccio. Essi passano attraverso insieme al solvente liquido.
La domanda dell'utente evidenzia un comune punto di confusione tra una soluzione e una miscela. La setacciatura è una tecnica basata sulla dimensione delle particelle, che la rende efficace per separare solidi grandi, non disciolti da un liquido, ma fondamentalmente incompatibile con le vere soluzioni dove le particelle solide sono di dimensioni molecolari.

Comprendere la natura di una soluzione
Particelle disciolte vs. non disciolte
Una vera soluzione è una miscela omogenea, il che significa che i componenti sono mescolati uniformemente fino al livello molecolare. Quando un solido come il sale si scioglie in acqua, la sua struttura cristallina si rompe.
I singoli ioni sodio e cloruro vengono circondati dalle molecole d'acqua. Queste particelle disciolte sono infinitamente piccole.
Perché la setacciatura fallisce per le soluzioni
Un setaccio funziona avendo pori di una dimensione specifica che consentono alle particelle più piccole di passare bloccando quelle più grandi.
Poiché gli ioni o le molecole disciolte in una soluzione spesso non sono più grandi delle molecole del solvente stesso, fluiscono attraverso la maglia del setaccio senza alcuna separazione. Sarebbe come cercare di catturare l'acqua con una rete da pesca.
Quando la setacciatura con liquidi è efficace
La setacciatura diventa un metodo valido quando si ha a che fare non con una soluzione, ma con una miscela eterogenea chiamata sospensione.
Il principio: significativa differenza di dimensioni
In una sospensione, le particelle solide sono insolubili e sono semplicemente disperse o sospese all'interno del liquido. La chiave è che queste particelle solide sono significativamente più grandi delle molecole liquide.
Questa differenza di dimensioni è ciò che consente a un setaccio, o a un filtro, di funzionare. I fori della maglia sono abbastanza piccoli da bloccare le particelle solide ma abbastanza grandi da far passare il liquido.
Esempi pratici di setacciatura
Questo principio è utilizzato in molte situazioni quotidiane:
- Separare ghiaia o sabbia dall'acqua.
- Scolare la pasta cotta dall'acqua.
- Rimuovere le foglie di tè dal tè infuso con un colino.
- Separare la polpa di frutta dal succo.
In tutti questi casi, il solido non è disciolto nel liquido; è semplicemente mescolato con esso.
Gli strumenti giusti per separare le soluzioni
Poiché la setacciatura è inefficace per le soluzioni, devono essere utilizzati altri metodi che si basano su diverse proprietà fisiche.
Evaporazione
Questo è il metodo più comune per recuperare un solido disciolto da un solvente liquido.
Riscaldando la soluzione, il solvente liquido si trasforma in gas ed evapora, lasciando dietro di sé il soluto solido. È così che il sale marino viene raccolto dall'acqua dell'oceano.
Distillazione
Se è necessario recuperare il solvente liquido (o sia il solvente che il soluto), la distillazione è la tecnica corretta.
La soluzione viene riscaldata per far bollire il solvente, il vapore risultante viene catturato e raffreddato in un condensatore, e si trasforma di nuovo in un liquido puro che viene raccolto separatamente. Il soluto solido rimane nel contenitore originale.
Scegliere il metodo di separazione giusto
La scelta della tecnica dipende interamente dalla natura della miscela.
- Se l'obiettivo è separare un solido insolubile da un liquido (una sospensione): La setacciatura (per particelle grandi) o la filtrazione (per particelle più fini) è l'approccio corretto.
- Se l'obiettivo è recuperare un solido disciolto da un liquido (una soluzione): Utilizzare l'evaporazione.
- Se l'obiettivo è recuperare il solvente liquido da una soluzione: Utilizzare la distillazione.
Comprendere se il solido è veramente disciolto o semplicemente sospeso è la chiave per selezionare lo strumento giusto per il lavoro.
Tabella riassuntiva:
| Tipo di miscela | Stato del solido | Metodo di separazione efficace |
|---|---|---|
| Soluzione | Disciolto (molecolare/ionico) | Evaporazione, Distillazione |
| Sospensione | Non disciolto (particelle grandi) | Setacciatura, Filtrazione |
Hai difficoltà a scegliere l'attrezzatura da laboratorio giusta per i tuoi processi di separazione? KINTEK è specializzata nella fornitura di attrezzature e materiali di consumo da laboratorio di alta qualità, inclusi sistemi di filtrazione e apparecchiature di distillazione, per aiutarti a ottenere separazioni precise ed efficienti. I nostri esperti possono aiutarti a selezionare gli strumenti perfetti per le esigenze specifiche del tuo laboratorio. Contattaci oggi per ottimizzare il tuo flusso di lavoro!
Guida Visiva