In una cella elettrolitica, la convenzione dei segni è definita dalla fonte di alimentazione esterna. All'anodo viene assegnato il segno positivo (+) e al catodo viene assegnato il segno negativo (-). Ciò è dovuto al fatto che viene applicata una tensione esterna per guidare una reazione chimica che non avverrebbe spontaneamente.
La chiave per comprendere una cella elettrolitica è riconoscere che non è un sistema autonomo. I segni dei suoi elettrodi sono dettati interamente dall'alimentatore esterno a cui è collegata, forzando il verificarsi di un cambiamento chimico non spontaneo.

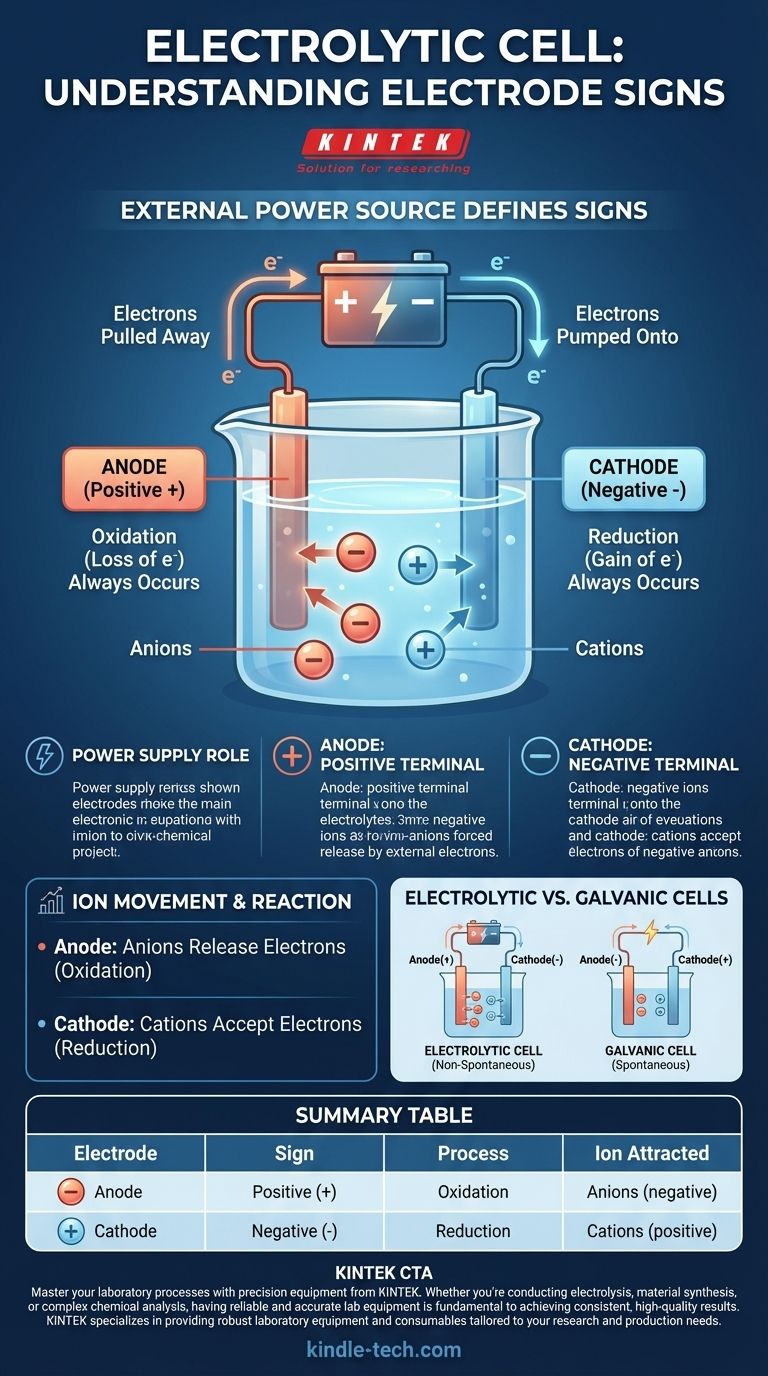
Perché una fonte di alimentazione esterna definisce i segni
Una cella elettrolitica utilizza energia elettrica per creare energia chimica. Questo processo, noto come elettrolisi, richiede una forza esterna—una batteria o un alimentatore CC—per avviare e sostenere la reazione.
Il ruolo dell'alimentatore
L'alimentatore agisce come una "pompa di elettroni". Tira gli elettroni da un elettrodo e li spinge verso l'altro, creando uno squilibrio di carica che costringe gli ioni nella soluzione elettrolitica a reagire.
L'anodo è collegato al terminale positivo
Il terminale positivo dell'alimentatore esterno è collegato all'anodo. Questo terminale attira attivamente gli elettroni lontano dall'anodo, lasciandolo con una carica netta positiva.
Il catodo è collegato al terminale negativo
Al contrario, il terminale negativo dell'alimentatore è collegato al catodo. Questo terminale pompa attivamente elettroni sul catodo, conferendogli un eccesso di elettroni e una carica netta negativa.
Come il movimento degli ioni crea la reazione
Le cariche forzate sugli elettrodi sono ciò che attira gli ioni disciolti nell'elettrolita, costringendoli a muoversi e reagire. Le definizioni fondamentali di ossidazione e riduzione rimangono costanti.
Anodo: il sito dell'ossidazione (sempre)
Indipendentemente dal tipo di cella, l'ossidazione (la perdita di elettroni) si verifica sempre all'anodo. In una cella elettrolitica, gli ioni a carica negativa (anioni) sono attratti dall'anodo positivo, dove rilasciano i loro elettroni in eccesso e vengono ossidati.
Catodo: il sito della riduzione (sempre)
Allo stesso modo, la riduzione (l'acquisizione di elettroni) si verifica sempre al catodo. Gli ioni a carica positiva (cationi) nella soluzione sono attratti dal catodo negativo, dove accettano gli elettroni in eccesso e vengono ridotti.
Una distinzione critica: celle elettrolitiche vs. galvaniche
Una fonte primaria di confusione sorge quando si confrontano le celle elettrolitiche con le celle galvaniche (o voltaiche), come una batteria standard. Le loro convenzioni di segno sono opposte per un motivo molto specifico.
Reazioni spontanee vs. non spontanee
Una cella galvanica funziona con una reazione chimica spontanea che produce energia elettrica. Qui, l'anodo è la fonte naturale di elettroni, rendendolo negativo, e il catodo è dove vengono consumati, rendendolo positivo.
Una cella elettrolitica esegue una reazione non spontanea che consuma energia elettrica. La fonte di alimentazione esterna inverte la polarità naturale per forzare il procedere della reazione.
La costante universale
Nonostante la differenza nei segni, i processi fondamentali sono gli stessi in entrambi i tipi di cella:
- L'anodo è sempre il sito dell'ossidazione.
- Il catodo è sempre il sito della riduzione.
Come ricordare i segni
Usa questi principi per mantenere chiare le convenzioni in base al tuo obiettivo.
- Se il tuo obiettivo principale è identificare i terminali: Ricorda che in una cella elettrolitica, i segni corrispondono all'alimentatore esterno: l'anodo è positivo e il catodo è negativo.
- Se il tuo obiettivo principale è tracciare gli ioni: Segui la semplice regola delle cariche opposte: gli anioni negativi si muovono verso l'anodo positivo e i cationi positivi si muovono verso il catodo negativo.
- Se il tuo obiettivo principale è distinguere i tipi di cella: Associa "elettrolitico" a una fonte di alimentazione esterna che forza una carica positiva sull'anodo e una carica negativa sul catodo per guidare la reazione.
In definitiva, i segni di una cella elettrolitica sono una conseguenza diretta di una fonte di alimentazione esterna che sovrascrive il flusso naturale di una reazione chimica.
Tabella riassuntiva:
| Elettrodo | Segno | Processo | Ione attratto |
|---|---|---|---|
| Anodo | Positivo (+) | Ossidazione | Anioni (negativi) |
| Catodo | Negativo (-) | Riduzione | Cationi (positivi) |
Padroneggia i tuoi processi di laboratorio con apparecchiature di precisione KINTEK.
Sia che tu stia conducendo elettrolisi, sintesi di materiali o analisi chimiche complesse, avere apparecchiature di laboratorio affidabili e accurate è fondamentale per ottenere risultati coerenti e di alta qualità. KINTEK è specializzata nella fornitura di apparecchiature e materiali di consumo di laboratorio robusti, adattati alle tue esigenze di ricerca e produzione.
Contatta oggi i nostri esperti per discutere come le nostre soluzioni possono alimentare le tue innovazioni e migliorare l'efficienza dei tuoi flussi di lavoro di laboratorio.
Guida Visiva
Prodotti correlati
- Cella Elettrolitica in PTFE Cella Elettrochimica Resistente alla Corrosione Sigillata e Non Sigillata
- Cella Elettrochimica Elettrolitica Super Sigillata
- Cella Elettrolitica Elettrochimica a Cinque Porte
- Cella Elettrolitica Tipo H Tripla Elettrochimica
- Cella Elettrochimica Elettrolitica a Diffusione di Gas Cella di Reazione a Flusso Liquido
Domande frequenti
- Quali sono le specifiche standard di apertura per tutte le celle elettrolitiche in PTFE? Una guida alle porte sigillate rispetto a quelle non sigillate
- Qual è la procedura corretta di spegnimento e smontaggio dopo un esperimento? Garantire la sicurezza e proteggere l'attrezzatura
- Qual è il metodo corretto per pulire la superficie di una cella elettrolitica interamente in PTFE? Garantire risultati accurati con una superficie incontaminata
- Quali precauzioni di sicurezza dovrebbero essere adottate durante un esperimento con la cella elettrolitica? Una guida per prevenire scosse elettriche, ustioni e incendi
- Quali sono i vantaggi dell'utilizzo di una cella elettrochimica in PTFE nella ricerca sugli attinidi? Garantire dati precisi sulla corrosione



















